
- UPSC IAS 預備考試化學筆記(第一部分)
- 化學 - 首頁
- 我們周圍的物質
- 我們周圍的物質是純淨的嗎
- 化學 - 原子與分子
- 化學 - 原子的結構
- 化學反應與方程式
- 化學 - 酸、鹼和鹽
- 材料:金屬和非金屬 I
- 化學 - 金屬與非金屬 II
- 碳及其化合物
- 元素週期律
- 合成纖維和塑膠
- 化學 - 煤和石油
- 化學 - 燃燒和火焰
化學 - 我們周圍的物質
引言
宇宙中發現的一切都是由某些物質構成的,科學家將其命名為“物質”。例如,我們吃的食物、我們呼吸的空氣、石頭、雲彩、星星、植物、動物、水、灰塵,所有這些都被歸類為物質。
物質微粒的特徵
物質的微粒非常小,通常肉眼無法看到。
物質的微粒在不斷地運動,這被稱為“動能”。
微粒的動能與溫度直接相關,溫度升高,運動速度也隨之增加。
物質的微粒之間存在吸引力,因此它們相互吸引。
微粒之間的吸引力將微粒結合在一起;但是,吸引力的強度因物質種類而異。
物質的狀態
物質有以下三種狀態:
固態
液態
氣態
讓我們簡要地討論一下:
固態
所有固體材料都具有確定的形狀、明顯的邊界和固定的體積。
大多數固體材料的壓縮性可以忽略不計。
所有固體材料在受到外力作用時都有保持其形狀的自然趨勢。
固體材料可以在外力作用下斷裂,但很難改變其形狀,因為它們是剛性的。
液態
與固體不同,液體沒有固定的形狀;但是,它們具有固定的體積。
液體佔據其所盛容器的形狀。
液體具有流動和改變形狀的特性。
氣態
以空氣形式存在的物質,既不是固體也不是液體,被稱為氣體。例如,氧氣、氮氣、氫氣等。
與固體不同,氣體沒有確定的尺寸和形狀。
諸如液化石油氣(LPG – 用於烹飪)和壓縮天然氣(CNG – 用於車輛燃料)等氣體具有很高的壓縮性;因此,大量的燃氣可以壓縮到一個小氣瓶中,便於運輸。
氣體通常表現出非常快地擴散到其他氣體中的特性。這就是為什麼我們可以聞到(無論是好聞的還是難聞的)遠處的氣味的原因。
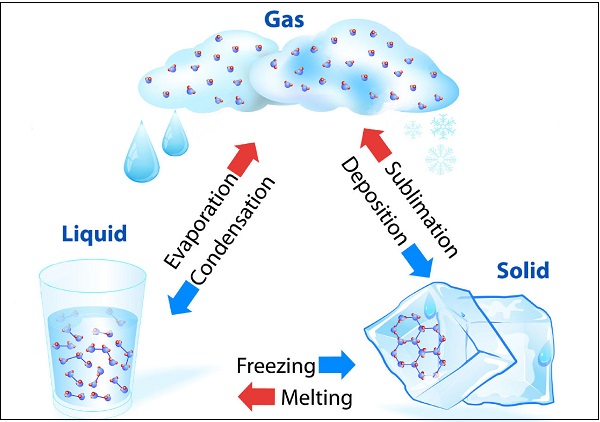
物質可以改變狀態
水可以以三種狀態存在,例如冰為固態;水(H2O)為液態;水蒸氣為氣態。下圖說明了水在不同狀態下的轉變:
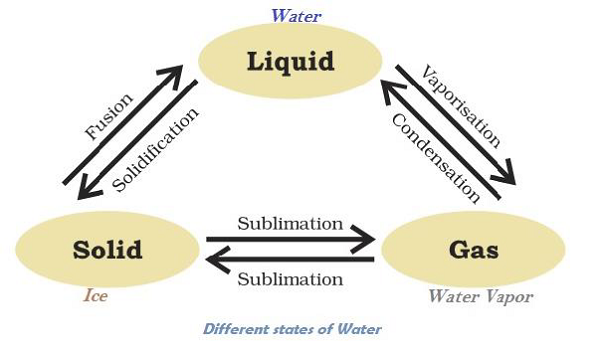
固體熔化並轉變為液體(在給定的大氣壓下)的溫度稱為“熔點”。
固體的熔點表明其微粒間吸引力的強度。
冰的熔點為 273.16 K,即 00 C。
熔化過程(即固態轉變為液態)稱為熔化。
在給定大氣壓下,將 1 kg 固體材料轉變為液體材料所需的熱能稱為潛熱。
液體在給定大氣壓下開始沸騰的溫度稱為“沸點”。
水的沸點為 373 K,即 1000C。
物質直接從固態轉變為氣態而不轉變為液態(反之亦然)的現象稱為“昇華”。
液體在低於其沸點的任何溫度下轉變為蒸汽的現象稱為“蒸發”。
固體二氧化碳 (CO2) 在高壓下儲存。

一旦壓力降低到 1 個大氣壓,固體 CO2 會直接轉化為氣態。
大氣壓 (atm) 是測量氣體施加壓力的單位,壓力的單位是帕斯卡 (Pa);1 個大氣壓 = 1.01 × 105 Pa。
物質的第四種狀態
等離子體是包含超高能和超激發粒子的一種狀態。

超激發粒子以離子化氣體的形式存在。例如,熒光管(包含氦氣)和霓虹燈(包含氖氣)包含等離子體。