
- UPSC IAS 預備考試化學筆記(第一部分)
- 化學 - 首頁
- 我們周圍的物質
- 我們周圍的物質是純淨的嗎
- 化學 - 原子與分子
- 化學 - 原子的結構
- 化學反應和方程式
- 化學 - 酸、鹼和鹽
- 材料:金屬和非金屬 I
- 化學 - 金屬與非金屬 II
- 碳及其化合物
- 元素的週期性分類
- 合成纖維和塑膠
- 化學 - 煤和石油
- 化學 - 燃燒和火焰
化學 - 化學反應與方程式
介紹
一種或多種化學物質與其他化學物質發生反應並轉化為一種或多種不同物質的過程稱為化學反應。
化學方程式
化學方程式是化學反應的符號表示;它透過符號和公式表示。例如
鎂 + 氧氣 = 氧化鎂
Mg + O2 = MgO
鎂和氧氣被稱為反應物,反應的結果,即氧化鎂被稱為產物。
記住,化學反應中產物中存在的元素的總質量必須等於反應物中存在的元素的總質量。
每種元素的原子數在化學反應前後始終保持不變。
化學反應的型別
以下是主要的化學反應型別 -
化合反應
分解反應
置換反應
讓我們簡要討論一下每個反應 -
化合反應
當兩種或多種物質(即元素或化合物)反應生成單一產物時,這種反應稱為化合反應。例如
CaO(s) +H2O(1)→Ca(OH)2(aq)
(生石灰) (熟石灰)
如上述反應所示,氧化鈣和水反應(或結合)生成單一產物,稱為氫氧化鈣。
在產物形成的同時也釋放熱量的化學反應稱為放熱化學反應。
分解反應
一種反應物分解成更簡單的產物的反應稱為分解反應。例如

在上述反應中,硫酸亞鐵晶體(即 FeSO4, 7H2O),加熱時會失去水分,晶體顏色發生變化。最後,它分解成氧化鐵 (Fe2O3)、二氧化硫 (SO2) 和三氧化硫 (SO3)。
置換反應
一種元素置換或去除另一種元素的反應稱為置換反應。例如
Fe(s)+ CuSO4(aq)→FeSO4(aq)+Cu(s)
(硫酸銅)(硫酸亞鐵)
在上述反應中,鐵從硫酸銅溶液中置換出銅並形成硫酸亞鐵。
氧化和還原
如果某種物質在反應過程中獲得氧氣,則稱為氧化。另一方面,在反應中,如果某種物質失去氧氣,則稱為還原。例如
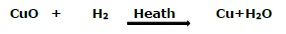
在上述反應中,氧化銅失去氧氣,因此被還原(即還原);另一方面,氫氣獲得氧氣,因此被氧化(即氧化)。
腐蝕
當金屬受到周圍環境中發現的物質(如水分、酸等)的侵蝕時,稱為腐蝕。例如,銀上的黑色塗層、銅上的綠色塗層等,

酸敗
當脂肪和油被氧化時,該過程稱為酸敗。它們的聞起來、嚐起來、顏色等也會發生變化;同樣,它使食物不適合食用。