氣體動理論假設
介紹
在日常生活中,我們經常觀察到光線透過小孔進入黑暗時空氣分子的運動。氣體動理論研究了空氣分子的運動。藉助動理論,可以根據氣體存在的容器的壓力(P)、體積(V)和溫度(T)來定義氣體的各種性質。微小粒子不會向上或向下移動,但它們可以向所有可能的方向移動。我們看不到這些粒子,因為它們的大小非常小,但我們能看到大粒子的運動。
Olivier Cleynen 和 User:Sharayanan,氣體動理論 (2),CC BY-SA 3.0
什麼是氣體動理論?
氣體包含大量大小可忽略不計的粒子,稱為分子。這些分子處於持續或不斷的運動狀態,或處於隨機運動狀態。在這次隨機運動中,分子不斷地以一定的速度運動,並與容器或其所存放容器的壁發生碰撞。
這些碰撞是完全彈性的,幾乎是瞬時的(持續時間很短),分子在碰撞之間以直線運動並獲得均勻的速度。
假設
粒子總是持續地向所有方向隨機移動,但其運動軌跡是直線。
粒子不受任何吸引力或排斥力的影響。
氣體是由大量具有小質量的微小粒子(如原子或分子)組成的集合。
粒子之間的空間非常大,因為粒子彼此相距很遠。因此,與容器的體積相比,粒子的體積可以忽略不計。
粒子總是處於不斷的運動狀態,因此它們具有動能,動能與溫度成正比。
由於微小粒子之間或與容器的碰撞,碰撞是完全彈性的,不會改變粒子的動量或能量。當粒子與容器碰撞時,也會對容器施加壓力。這個壓力取決於單位面積上碰撞的粒子數量。
動能和壓力
我們知道動量是質量和速度的乘積。
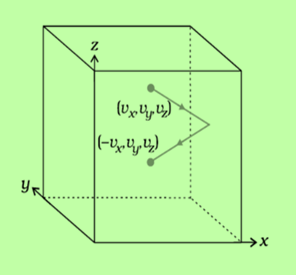
圖2:分子在不同分量上的運動
分子動量的變化
$\mathrm{\Delta P=P_2-P_1}$
$\mathrm{\Delta P=mv_x-(-mv_x)}$
$\mathrm{P=2mv_x}$
連續碰撞的時間 $\mathrm{t=\frac{2A}{V_x}}$ 所以作用在壁上的力為
$\mathrm{F=\frac{\Delta P}{\Delta t}}$
$\mathrm{F=\frac{2mv_x}{2Av_x}}$
$\mathrm{F=m v_x^{2}}$
x方向上的壓力,$\mathrm{P_x=\frac{F_x}{A}=\frac{m}{A^3}(v_x^{2})}$
同樣,對於y方向 $\mathrm{P_y=\frac{m}{A^3}(v_y^{2})}$
以及對於z方向,$\mathrm{P_z=\frac{m}{A^3}(v_z^{2})}$
根據帕斯卡定律:
$\mathrm{P_x=P_y=P_z=P}$
我們可以寫成,$\mathrm{P=\frac{P_x+P_y+P_z}{3}}$
現在代入所有方向的壓力:
$\mathrm{P=\frac{m}{3A^3}(v_x^{2})+\frac{m}{3A^3}(v_y^{2})+\frac{m}{3A^3}(v_x^{2})}$
$\mathrm{P=\frac{m}{3A^3}(v_x^{2}+v_y^{2}+{v_z}^2)}$
$\mathrm{P=\frac{m}{3A^3}(v_{RMS}^2)}$
此外,我們可以寫成,$\mathrm{P=\frac{1}{3}\rho (v_{RMS}^2).......(1)}$
其中 $\mathrm{v_{RMS}}$ - 均方根速度
$\mathrm{\rho}$ - 分子的密度
單位體積的動能:
$\mathrm{E=\frac{1}{2}\rho v^2...…(2)}$
將方程式 (1) 和 (2) 相除
$\mathrm{\frac{P}{E}=\frac{\frac{1}{3}\rho (v_{RMS}^2)}{\frac{1}{2} \rho v^2}=\frac{2}{3}}$
$\mathrm{P=\frac{2}{3}E}$
所以壓力 $\mathrm{=\frac{2}{3}}$ 單位體積的動能
動能和溫度
根據動理論
$\mathrm{P=\frac{1}{3}\rho (v_{RMS}^2)}$
$\mathrm{\rho=\frac{M}{v}}$
$\mathrm{P=\frac{1M}{3v}(v_{RMS}^2)}$
乘以併除以2
$\mathrm{PV=\frac{2}{3}\frac{1}{2}m(v_{RMS}^2)}$
$\mathrm{PV=\frac{2}{3}E}$
(我們知道 1 摩爾的理想氣體方程 PV=RT)
$\mathrm{RT=\frac{2}{3}E}$
$\mathrm{E=\frac{3}{2}RT}$
每個分子的平均動能
$\mathrm{\overline{E}=\frac{E}{N}=\frac{3}{2}\frac{R}{N}T=\frac{3}{2}K_B T}$
N - 阿伏伽德羅常數
弛豫時間
這也被稱為平均自由時間。粒子的運動是完全隨機的。在它們的運動過程中,它們會發生碰撞並改變方向。每次碰撞都會使它們隨機改變方向。
因此,在兩次連續碰撞之間,兩個粒子之間的平均時間或時間間隔稱為弛豫時間。
平均自由程
在兩次連續碰撞之間,分子以恆定速度沿直線路徑運動。粒子相遇另一個粒子所走過的平均距離。並非每個路徑長度或自由程都是相同的。它可能因不同的粒子而異。它用“λ”表示。
平均自由程:
$\mathrm{\lambda=\frac{1}{\sqrt{2}\pi d^2 \frac{N}{V}}(其中\:n=\frac{N}{V})}$
$\mathrm{\lambda=\frac{1}{\sqrt{2}\pi d^2 n}}$
其中 n 是單位體積內的分子數
d 是分子的直徑
布朗運動
圖片即將推出
圖3:布朗運動
如果細小的粒子(原子或分子)懸浮(散佈)在任何流體(液體或氣體)中,它們就會開始向所有可能的方向進行隨機運動,並彼此碰撞,並與它們所保持的容器碰撞,形成鋸齒狀路徑。這種運動稱為布朗運動。
植物學家羅伯特·布朗於 1827 年首次描述了這種運動,因此為了紀念他,這種運動被稱為布朗運動,當時他用顯微鏡觀察浸在液體中的花粉粒。
後來在 1905 年,愛因斯坦提出了他的布朗運動理論。花粉粒由於粒子的碰撞或轟擊而隨機移動。這就是愛因斯坦在他的論文中所展示的。讓·佩蘭證實了這一解釋,並因此獲得了 1926 年的諾貝爾獎。在陽光照射到佈滿灰塵的房間時,可以觀察到一些現象。我們觀察到灰塵粒子隨機移動。
結論
氣體動理論有助於理解粒子的宏觀性質或微觀性質。透過知道溫度,我們可以很容易地找到平均動能,因為動能與溫度成正比。所有這些都可以在原子理論中進行研究。氣體動理論的結論是粒子總是在運動。
常見問題
Q1。均方根分子速度取決於哪些量?
答:我們知道,$\mathrm{v_{RMS}=\sqrt{\frac{3RT}{M}}}$
氣體的速度是
與絕對溫度成正比
與氣體的摩爾質量成反比
此外,$\mathrm{摩爾質量=\frac{體積}{摩爾}}$
$\mathrm{摩爾質量=\frac{體積}{\frac{質量}{M}}}$
因此,摩爾體積與氣體的均方根速度成正比。
Q2。一輛裝有貨物的卡車以均勻速度行駛。放在卡車上的罐裝氣體內部的氣體分子溫度是多少?
答:分子獲得相對速度,均方根速度與橫向平移不同。
Q3。氣體分子平均動能取決於哪些因素?
答:氣體原子或分子的平均動能取決於溫度,因為動能與絕對溫度成正比。
$\mathrm{K=\frac{3}{2}\frac{R}{N_A}T}$
Q4。如果氫氣和氧氣樣品的體積相同,那麼哪個樣品的分子數量更多?
答:如果兩個樣品的體積相同,則氣體的溫度和壓力相同。結果,兩個樣品的分子數量相同。
Q5。氫 (H) 分子的溫度和均方根速度在 79°C 時等於氧 (O) 分子的溫度和均方根速度。
答:我們知道:
$\mathrm{v_{RMS}=\sqrt{\frac{RT}{M}}}$
氧分子的均方根速度等於氫的均方根速度。
$\mathrm{\sqrt{\frac{273+79}{32}}=\sqrt{\frac{T}{2}}}$
$\mathrm{\frac{352}{32}=\frac{T}{2}}$
$\mathrm{11\:\times\:2=T}$
$\mathrm{T=22^{\circ}C}$
因此需要 22°C 的溫度。


 資料結構
資料結構 網路
網路 關係型資料庫管理系統 (RDBMS)
關係型資料庫管理系統 (RDBMS) 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C語言程式設計
C語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP