反應型別實驗
介紹
在粒子參與化學反應的過程中,可能會觀察到不同型別的反應實驗。在這個反應或實驗中,可能會發生內部和外部變化。在這些型別的反應中,主要物質的物理性質不會發生變化,例如,熔點或蒸發溫度的變化等。
什麼是反應實驗?
反應實驗是化學領域的一個組成部分,不同的反應型別被安排以形成新的分子或改變物理和化學物質。
化學領域的興奮完全取決於分子反應能力。
可以看到各種各樣的實驗,對於這些反應,實驗過程也各不相同。化合反應和分解反應是化學領域中最有用和最常用的實驗。單置換反應實驗以及燃燒反應是化學領域中其他非常重要的反應型別。
化合反應
這種反應需要兩種不同的分子發生反應,然後形成一種新的化合物。這種型別的反應也稱為合成反應,因為在單一反應中,會發生雙分子或多個粒子的重排和結合以形成產物。這種反應型別的一個簡單例子如下所示:
$$\mathrm{X+Y = XY}$$
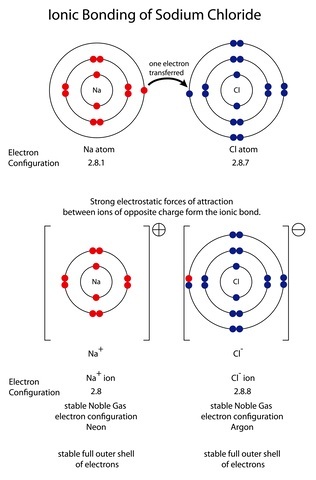
圖1:NaCl 的形成
這種反應型別的真例項子是 NaCl 的形成,在這個反應中,鈉和氯反應形成氯化鈉。該反應表示為:
$$\mathrm{2\:Na (s) + Cl_2 (g)\:\rightarrow\:2NaCl (s)}$$
這種反應型別的另一個實驗是在 $\mathrm{O_2}$ 中看到的,在這個反應中,金屬或非金屬物質與氧反應形成氧化物。該反應表示為:
$$\mathrm{2\:Mg (S) + O_2 (g)\:\rightarrow\:2MgO (s)}$$
分解反應
這種型別的反應與之前的反應略有不同。在這個反應中,一個複雜的分子分解成一個簡單的分子。分解實驗需要一個特定的能源,這對於破壞分子中現有的鍵至關重要。它表示化合物分解成簡單的化合物或分子。這種反應型別的一個例子如下所示:
$$\mathrm{XY = X+Y}$$
它主要發生在不同的自然資源中,如光、熱和電。當二元分子直接組合形成新產物時,就會發生簡單的分解反應。一個例子如下所示:
$$\mathrm{2\:HgO (s)\:\rightarrow\:2\:Hg (l) + O_2 (g)}$$
它表明反應物可以很容易地轉化為特定形式。該形式可以是元素或化合物。透過該過程,$\mathrm{CaCO_3}$ 會分解成一些分子,如氧化鈣和二氧化碳。鹼和鹼在加熱後很容易分解。該反應表示為:
$$\mathrm{2\:NaOH (s) \:\rightarrow\: Na_2O (s) + H_2O (g)}$$
單置換反應實驗
這是一種複雜的化合物型別,在這個反應中,反應物中的單個元素被另一種型別的各種反應物的元素取代。它也稱為單置換反應實驗,因為它依賴於分子的化學反應性。在這個反應中,高反應性元素主要被低反應性元素取代。它表示為:
$$\mathrm{X+YZ = XY+Z}$$
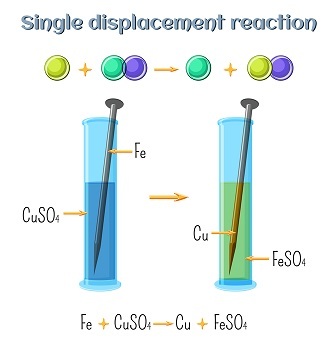
圖2:金屬鐵置換銅離子的反應
在這個實驗中,鎂和銅之間可以看到一個例子,在這個反應中,鎂主要取代銅,因為鎂的反應能力高於銅。該反應可以表示為:
$$\mathrm{Mg\:(s) + Cu(NO_3)_2 (aq)\:\rightarrow\: Mg(NO_3)_2\:(aq) + Cu\:(s)}$$
這種反應型別的另一個例子如下所示:
$$\mathrm{Fe(s) + CuSO_4(aq)\:\rightarrow\:FeSO_4(aq) + Cu(s)}$$
燃燒反應
這種型別的反應是一種特殊的化學實驗,其中反應物在氧的幫助下參與反應,然後釋放一定量的能量和熱量。這種反應主要發生在氧的存在下,可以看到兩種不同型別的反應,即不完全燃燒和完全燃燒。
它表明有機分子發生完全燃燒,產生氣態 $\mathrm{CO_2}$ 和 $\mathrm{H_2O}$ 並釋放能量。該反應表示為:
$$\mathrm{C_3H_8 (g) +5O_2 (g)\:\rightarrow\:3CO_2 (g) + 4H_2O (g)}$$
這表明烴類在這種反應中被用來產生能量。這種型別的反應被稱為放熱反應。
結論
反應不僅在實驗室中可以看到,在周圍環境中也可以看到。所有反應或實驗的持續時間並不相同。新增催化劑後,不同分子的反應速率會發生變化。反應中通常不會看到任何型別的物理變化。
常見問題
Q1. 什麼叫雙置換反應?
答:這種型別的化學反應具有正離子和負離子,它們交換位置以形成新的化合物。它主要發生在離子化合物中,該反應表示為:
$$\mathrm{AB + CD\:\rightarrow\:AD + CB}$$
Q2. 單置換反應和雙置換反應的區別是什麼?
答:在單置換反應中,只有一個化合物被其他兩個依賴於反應活性的反應物取代。雙置換反應指導反應物陽離子以及陰離子交換的反應。
Q3. 什麼叫金屬的反應活性序列?
答:反應活性序列是指將金屬按反應活性遞減順序排列的序列。氫是該序列中唯一的非金屬元素,用於比較。


 資料結構
資料結構 網路
網路 關係資料庫管理系統 (RDBMS)
關係資料庫管理系統 (RDBMS) 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C語言程式設計
C語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP