酮的製備
引言
羰基 (𝑪 = 𝑶) 存在於稱為酮的化學分子中。酮是反應迅速的化學物質。酮和醛關係密切,但酮的反應活性比醛弱。
酮的不均勻電荷分佈導致其極性特徵。酮是許多構建塊的基礎。它可以用於製造紡織品、溶劑(用於製造炸藥)、油漆、清漆等。酮還用於水力壓裂劑的處理、修復和染色。實驗室和工業規模上經常使用多種酮的製備方法。
什麼是酮?
酮可以被認為是有機化合物,含有羰基,即一個碳原子與一個氧原子連線,其餘鍵與烴基相連。在酮的情況下,兩個 R 基團連線到羰基(𝑪 = 𝑶)。酮基存在於消炎藥中。
酮的結構
在化學中,酮是一個官能團,其化學式為$\mathrm{R_{2}C\:=\:0}$。酮中的羰基碳通常被稱為“𝒔𝒑𝟐雜化”。酮圍繞酮羰基碳呈三角平面形,具有約120°的碳-碳-碳鍵角和碳-碳-氧鍵角。與醛不同,酮分子中羰基 (𝑪𝑶) 連線到碳骨架中的兩個碳原子。
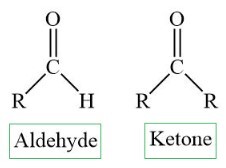
酮的反應
酮被認為是化學中最高反應活性的物質之一。然而,酮比醛不那麼活潑和反應性。考慮到羰基是所有化學反應的基礎,酮和醛是相似的。酮的極性特徵是由其不均勻的電荷分佈引起的。不均勻的排列導致碳原子上帶正電荷。以下是酮的一些重要反應:
親核試劑對酮羰基的進攻。 −
親核試劑加到羰基的親電碳上。隨後進行質子化,形成𝑂 − 𝐻鍵。

酮與氨或1°胺反應可以生成亞胺。 −
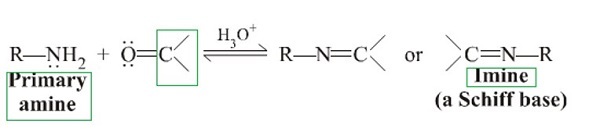
與醇的反應
當酮與醇或醇鹽反應時,會生成半縮酮或其相應的鹼。二醇轉化為縮酮。此反應用於保護酮。
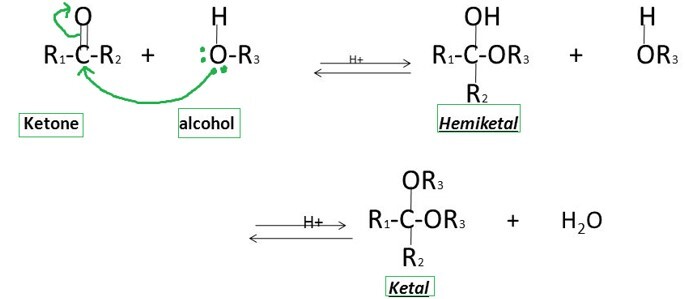
酮與強氧化劑反應生成羧酸。 −
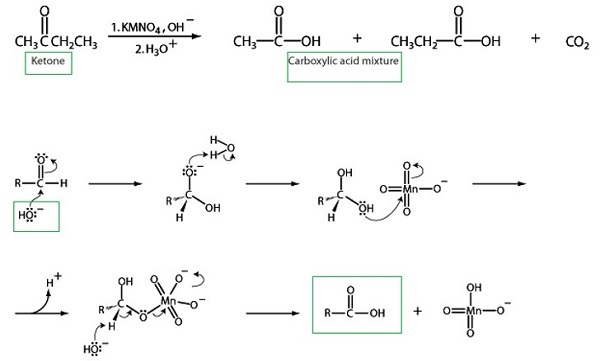
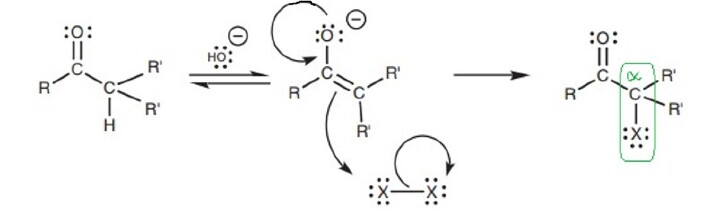
與鹵素的反應 −
烯醇作為介質,將酮轉化為α-滷代酮。
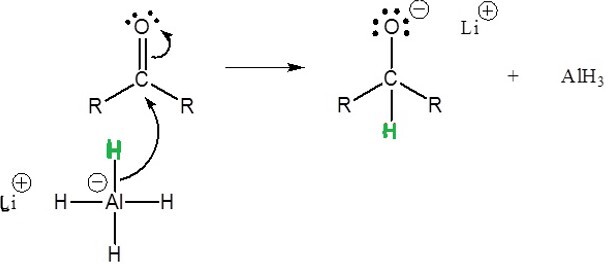
與還原劑的反應 −
酮與還原劑如$\mathrm{LiAlH_{4}}$反應生成仲醇。
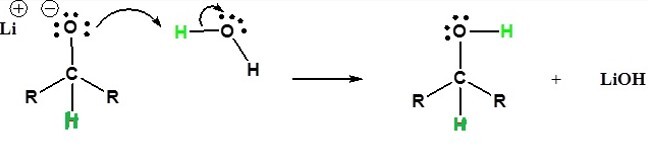
酮的鑑定
透過化學名稱 − 僅透過其化學名稱即可鑑定酮。化學名稱末尾的“one”字尾表示酮的存在。
透過溶解度 − 必須研究溶液在水中的溶解度和沸點,根據其物理特性來確定酮。如果它是關鍵成分,則其在水中的溶解度和沸點都將非常重要。
透過光譜 − 酮和醛在接近1700 𝒄𝒎−𝟏的紅外波長處強烈吸收。根據組成,13𝐶 𝑁𝑀𝑅譜顯示訊號略微向下場移動到200 ppm。
有機試劑 − 酮在2,4-二硝基苯肼試驗(布拉迪試驗)中呈陽性結果,在費林溶液或託倫試劑試驗中呈陰性結果。
酮的製備
在化學實驗室和工業規模上,經常使用多種酮的製備方法。以下是其中一些方法:
由腈製備酮
透過這種方法,可以使用格氏試劑作用於腈來製備酮。格氏試劑將靶向腈中的親電碳中心以生成亞胺鹽。生成的溶液必須經過水解才能得到酮作為產物。

格氏試劑與腈在水性酸中反應,會生成酮,同時產生氨和鎂鹽作為副產物。
透過醇的脫氫製備酮
如果從相應的醇分子中去除一個氫分子,則醇會發生脫氫反應。在氧化過程中,C − O和O − H強的鍵被還原為純粹的C = O鍵。因此,需要仲醇的脫氫來形成酮。
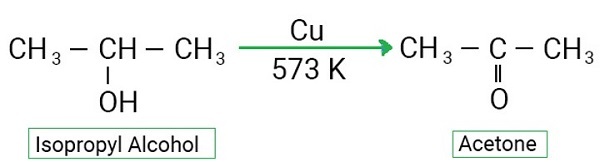
然而,對於叔醇,由於在這種情況下不存在α-氫,因此應在有機物的氧化之後用脫水過程代替脫氫過程。

由醯氯製備酮
一旦格氏試劑與醯氯反應後暴露於強金屬鹵化物中,酮就會合成。例如,當氯化鎘被迫與敏感試劑反應時,會產生二烷基鎘。此後產生的產物準備好與醯氯反應生成酮。
反應 −
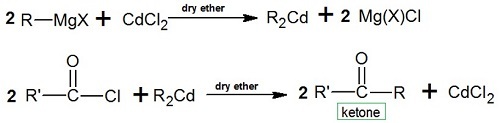
該過程的機理如下所示

由苯和取代苯製備酮
苯及其取代形式易於生成芳香酮。這被認為是化學中製備芳香酮最有效的方法。該方法包括用醯氯處理苯以生成酮。只有催化劑(例如路易斯酸,如用醯氯處理的苯$\mathrm{AlCl_{3}}$)的存在才能使這種反應成為可能。
反應 −
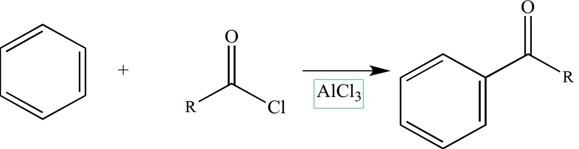
該過程的機理如下所示
步驟1 − 親電試劑的形成。

步驟2 − 親電試劑對苯環的進攻。
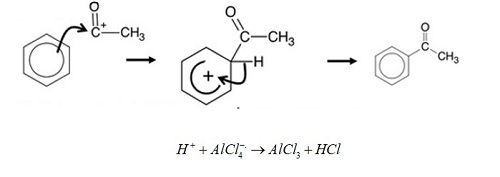
結論
酮的標準式為𝑹(𝑪 = 𝑶)𝑹′,其中 R 和 R' 可以是烷基或芳基。根據其取代基,它們分為兩種型別:酮的對稱形式和不對稱形式。酮可以透過多種方法大量製備,並在實驗室中製備。烴、醇和其他化合物經常發生氧化反應生成酮。
常見問題解答
1. 哪種方法不使用烷基腈來製備酮?
烷基腈不能在酸中水解以釋放酮。
2. 什麼可以還原酮?
幾種還原劑可以還原醛和酮。兩種主要的還原劑是硼氫化鈉和氫化鋁鋰。
3. 為什麼酮不氧化?
酮不易氧化,因為它們的羰基不含氫原子。酮只能被非常強的氧化劑(如高錳酸鉀溶液)氧化。
4. 為什麼酮的反應速度比醛慢?
因為酮中的兩個烷基顯著降低了羰基碳的親電性,比醛中的親電性低,所以酮比醛活性低。
5. 為什麼酮的沸點比醛高?
酮的沸點比異構醛略高。這是因為羰基碳被兩個給電子基團包圍,使其更極性。


 資料結構
資料結構 網路
網路 關係資料庫管理系統 (RDBMS)
關係資料庫管理系統 (RDBMS) 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C語言程式設計
C語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP