炔烴的物理性質
簡介
炔烴是由碳和氫組成的最基本的無機分子。碳氫化合物是自然界中存在的東西,也是人們日常生活中使用的任何東西中都存在的東西。這就是它們被認為是母體有機化合物的原因。任何化合物都可以透過取代氫原子來製備。
什麼是炔烴?
炔烴可以定義為非極性不飽和烴,碳原子之間存在三鍵,可以表示為 -C≡C-。其通式為 $\mathrm{C_nH_{2n–2}}$,其中 n 的值可以變化;可以是 2、3、4、5 等等。
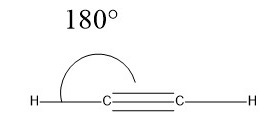
圖 1:炔烴:乙炔
最簡單的炔烴至少有一個三鍵。炔烴也被稱為乙炔。然而,這個名稱有時僅指一種炔烴,即 C2H2。炔烴也被稱為乙醯基,並且是疏水的。
炔烴的結構
炔烴的鍵意味著 H–C≡C 鍵角形成 180° 角,並且由於該角,它們看起來像一根杆。其三鍵非常強,以至於“鍵能為 839 kJ/mol。然而,鍵合是根據分子軌道理論討論的,其中三鍵被認為是由 s 和 p 軌道的重疊產生的。
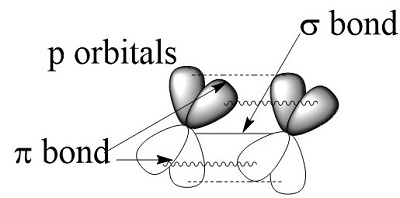
圖 2:炔烴的結構
根據 IUPAC 框架,隨著 $\mathrm{C_nH_{2n–2}}$ 中 n 的變化,每種炔烴的名稱以特定的方式形成。它們都帶有後綴 -yne,字首取決於碳原子數。例如,乙炔的碳原子數為 2,其化學式為 $\mathrm{C_2H_2}$,丁炔也是如此,其中碳原子數為 4,其化學式為 $\mathrm{C_4H_6}$。
其他一些炔烴有:丙炔、戊炔、己炔、庚炔、辛炔,它們的碳原子數分別為 3、5、6、7、8。
炔烴的異構現象
炔烴的結構異構主要有四種類型,它們是:
鏈異構:這種異構發生在炔烴具有五個或更多碳原子,並且由於各種碳鏈構型而產生的。
位置異構:在這種異構中,異構體根據三鍵的位置而不同。
官能團異構:在這種異構中,二烯的官能團異構體是含有兩個雙鍵的化合物。
環鏈異構:在這種異構中,它們與環烷烴表現出環鏈異構。
炔烴的物理性質
炔烴最常見的物理性質與烷烴和烯烴有些相似:
炔烴的物理狀態
它們是不飽和碳,在碳位點具有三鍵。該組的前三個成員是無色的,以氣體形式存在,而其餘八個成員是液體,除此之外,較高階的炔烴以固體形式存在。炔烴本質上是輕微的極性。
氣味或臭味
所有炔烴成員都是無臭的,但乙炔具有大蒜樣氣味。其背後的原因是磷化氫雜質的存在。除此之外,乙烯具有輕微的氣味。
炔烴的沸點和熔點
炔烴的熔點和沸點取決於分子量。這兩個點隨著分子量的增加而增加。如果將炔烴的熔點和沸點與烷烴和烯烴進行比較,則它們更高。
溶解度
炔烴在非極性溶劑中表現出可溶性,而在極性溶劑(如水)中不溶。
密度
炔烴的密度隨著分子量的增加而增加。如果可以與水進行比較,它們是輕的。炔烴的密度範圍為 0.69–0.77 g/cm3。
炔烴的用途
炔烴用於許多行業,例如:
乙炔具有極高的火焰,因此它們被用於氧乙炔氣體焊接和切割。
它們被用作燃料。
它用於製造天然混合物,例如乙醇、乙酸和丙烯酸。
它們被用作氣體燈。
乙炔用於使水果成熟。
它們用於製造順式和反式烯烴。
結論
炔烴具有獨特的結構,這使其與其他化合物不同,並且在有機化學領域至關重要。它們主要有兩種型別,即末端炔烴和內炔烴。與任何其他碳氫化合物一樣,炔烴本質上也是疏水的。
常見問題
Q1. 炔烴的主要性質是什麼?
答:炔烴是不飽和烴,其物理性質與烷烴和烯烴相似。其中最重要的是 - 溶解於有機溶劑,並且在極性溶劑中稍微溶解。然而,它們不溶於水。
Q2. 炔烴具有酸性嗎?
答:炔烴本質上是酸性的,其原因是它們可以“釋放氫原子,然後可以形成炔負離子。由於炔烴的酸性,它們可以用作布朗斯臺德-勞裡酸”。
Q3. 炔烴的主要用途是什麼?
答:炔烴被用作幫助洞穴探險的燈籠。它也用作氧乙炔炬的燃料。由於其能夠產生高溫,因此它在焊接和切割金屬方面是首選。
Q4. 為什麼炔烴具有較高的沸點?
答:炔烴的沸點隨著分子量的增加而升高。不僅如此,熔點也會因此而升高。


 資料結構
資料結構 網路
網路 關係資料庫管理系統
關係資料庫管理系統 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C 語言程式設計
C 語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP