構象異構體
引言
構象異構體,也稱為構象異構物,是立體異構體的一種(一種分子具有相同的分子式但在空間中原子具有不同的三維取向的異構體),其中異構體可以透過繞其單鍵或σ鍵旋轉輕鬆相互轉化。
並且這些轉化可以在室溫下進行。這是因為改變或轉換一種構象異構體形式為另一種形式所需的能量通常不足,因此轉化可以在室溫下輕鬆發生。構象異構體的一些例子包括**乙烷、正丁烷**等。
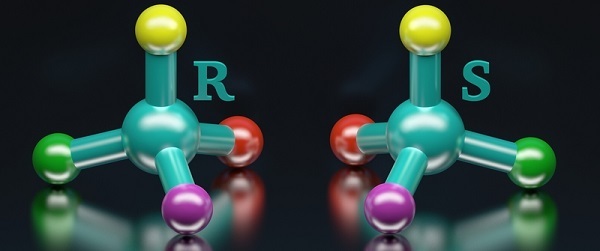
什麼是構象?
構象定義為分子中所有可能的原子空間或三維排列的任何一種或多種,這是由於其原子組成基團繞σ鍵或單鍵旋轉或扭曲造成的。任何具有連線或連線兩個多原子基團的單共價鍵的分子都可能存在不同型別的構象或構象異構物,並且在每一個構象異構物中,都至少存在一個原子不位於分子中該單鍵的軸線上或附近。
最簡單的例子之一是過氧化氫;在這裡,兩個羥基可以繞氧-氧鍵的軸線彼此輕鬆旋轉或扭曲。並且同一分子的每一個不同的構象都突出或代表一個具有不同勢能的狀態。
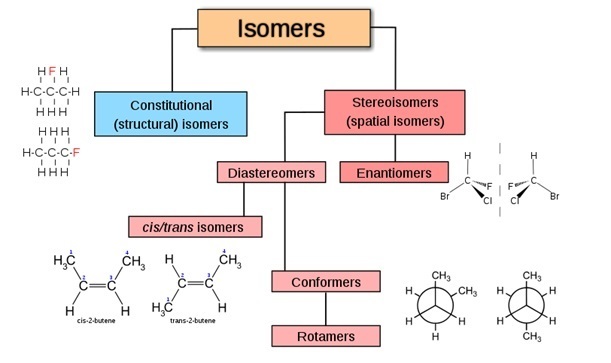
Vladsinger,異構體,CC BY-SA 3.0
構象異構體
構象異構體也稱為旋轉異構體或構象異構物。這些是立體異構體(具有相同分子式或經驗式但其原子的空間或三維排列不同的異構體)由於繞其軸線的σ鍵或單鍵的旋轉或扭曲而產生的。在構象異構體中,異構體可以透過繞σ鍵或單鍵旋轉輕鬆相互轉化。並且這些轉化可以在室溫下進行,因為從一種形式轉換為另一種形式所需的能量非常低。一些構象異構體或排列根據相鄰基團之間形成的二面角指定一些特定的符號。例如,乙烷的交叉式、偏斜式和重疊式,正丁烷的反式或鄰式構象。

乙烷的不同形式基於它們的二面角。

重疊式和交叉式構象的表示
**重疊式構象** - 這種構象是由於分子中原子或原子基團的排列之間形成0°二面角造成的。由於這種原子的排列方式,這種構象的穩定性非常低。在這裡,鍵電子對經歷高排斥,因為原子或原子基團之間沒有空間。由於穩定性低,分子具有較高的勢能。

Dissolution,交叉式和重疊式,CC BY-SA 3.0
**交叉式構象** - 這種構象是由於分子中原子或原子基團的排列之間形成60°二面角造成的。由於這種原子的排列方式,這種構象的應變非常低。
在這裡,鍵電子對經歷非常低的排斥,因為原子或原子基團之間有空間。因此,這是最穩定的構象。由於高穩定性,分子具有較低的勢能。
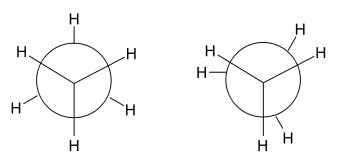
Dissolution,交叉式和重疊式,CC BY-SA 3.0
鋸齒式投影
鋸齒式投影是從一個角度而不是從側面投影分子的投影。這種投影類似於紐曼投影,但不同之處在於這種投影顯示了分子中間的碳-碳(C-C)鍵。而且,我們也可以在重疊式或交叉式構象中繪製這種型別的投影。在這種型別的投影中,不需要一直顯示氫原子。
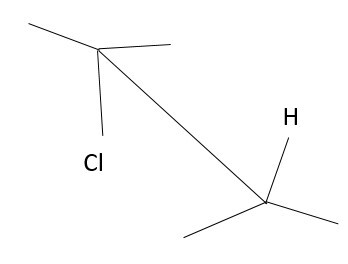
紐曼投影
紐曼投影是從前到後出現的化學鍵的基本視覺化,前面存在的原子用點表示,而圓圈表示後面的原子。這種投影在烷烴的立體化學中起著非常重要的作用。在這種投影中,前面存在的碳原子稱為“近端碳”,後面存在的碳原子稱為“遠端碳”。這種紐曼投影對於確定前後(近端和遠端)碳原子的二面角也很有用。
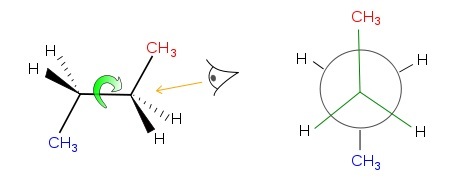
I,Amelliug,紐曼,CC BY-SA 3.0
結論
構象異構體也稱為構象異構物或旋轉異構體,是具有相同分子式但原子或原子基團的空間排列不同的異構體,它們透過在室溫下繞σ鍵或單鍵旋轉從一種形式轉換為另一種形式。重疊式構象異構體是由於分子中原子或原子基團的排列之間形成0°二面角造成的,而交叉式構象異構體是由於分子中原子或原子基團的排列之間形成60°二面角造成的。鋸齒式投影是分子的角度投影,而紐曼投影是分子的側面投影。
常見問題
1. 什麼是構象異構物?
構象異構物,也稱為構象異構體,是由於分子中σ鍵或單鍵的旋轉而產生的相同分子的不同形式的異構體。
2. 為什麼構象異構體的相互轉化在室溫下是可能的?
在構象異構體中,從一種形式到另一種形式的相互轉化在室溫下是可能的,因為轉化所需的能量不足。
3. 二面角是什麼意思?
二面角是由兩個平面相互交叉形成的角度。並且,兩個相交平面是笛卡爾座標系。
4. 重疊式和交叉式形式中分別存在的二面角是多少?
在重疊式形式中,二面角為0°;對於交叉式形式,二面角為60°。
5. 鋸齒式投影和紐曼投影之間的基本區別是什麼?
鋸齒式投影是從一個角度投影分子,而紐曼投影是分子的側面投影(偏轉影像)。


 資料結構
資料結構 網路
網路 關係型資料庫管理系統(RDBMS)
關係型資料庫管理系統(RDBMS) 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C語言程式設計
C語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP