(a) 書寫從其碳酸鹽礦石中提取中等活潑性純金屬的步驟。(b) 銅是如何從其硫化礦石中提取的?解釋各個步驟並提供化學方程式。繪製銅電解精煉的帶標籤示意圖。
(a) 鐵、鋅、鉛、銅等為中等活潑金屬,以硫化物或碳酸鹽形式存在,可透過還原或電解從礦石中獲得。
例如,鋅礦石在空氣中進行富集和焙燒,生成氧化鋅和一氧化碳。當ZnCO3在空氣中焙燒時,會形成CO2。
反應方程式如下所示
$ZnCO_{3}(s)\rightarrow ZnO(s)+CO_{2}(g)$
然後將從礦石中產生的氧化鋅與碳一起加熱以將其還原為金屬鋅。
$ ZnO(s) + C\rightarrow Zn(s)+CO(g)$
(b) 以下是從硫化礦石中提取銅的步驟
1) 礦石富集:採用浮選法去除不需要的金屬和脈石以提純礦石,因為它是硫化礦石。
2) 焙燒:輝銅礦 (Cu2S) 在空氣中焙燒。$2Cu_{2} S( s) +3O_{2}( g) \ \rightarrow 2Cu_{2} O( s) +2SO_{2}( g)$
3) 還原:然後在無空氣的情況下加熱氧化銅。用硫化亞銅還原氧化亞銅
$2Cu_{2} O+Cu_{2} S\rightarrow 6Cu( s) +SO_{2}( g)$
此反應稱為自還原。
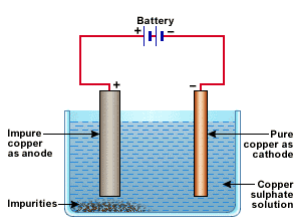
4) 電解精煉反應:將不純的銅金屬製成陽極,將純銅製成陰極,並使用硫酸銅作為電解液。電解液中的純銅沉積在陰極上,可溶性雜質進入溶液,不溶性雜質保留在溶液中並沉積在陽極底部。
$陽極:Cu^{2+}( aq) +2e^{-}\rightarrow Cu( s)$
$陰極:Cu( s) \ \rightarrow Cu^{2+}( aq) +2e^{-}$

廣告

 資料結構
資料結構 網路
網路 關係資料庫管理系統 (RDBMS)
關係資料庫管理系統 (RDBMS) 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C語言程式設計
C語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP