等溫膨脹
引言
等溫過程是一種熱力學過程,其中系統的溫度 (T) 保持恆定 (c),即 ΔT=0。這種過程通常發生在系統與外部熱庫接觸,並且系統變化足夠緩慢,允許系統透過熱量 (ΔH) 交換持續調整到熱庫的溫度 (T)。
對於理想氣體,分子或原子之間所有的碰撞都是**完全彈性**的,理想氣體中不存在分子間的吸引力,因為理想氣體分子運動速度很快,並且彼此相距很遠,因此它們不會相互作用。因此,它們可以在恆溫下輕鬆膨脹。
什麼是等溫膨脹?
等溫膨脹定義為氣體(或空氣)在一定恆溫 (T) 下的膨脹。由於空氣在膨脹時對環境做功 (w),因此會損失熱量,因此必須向空氣新增或提供熱量 (ΔH) 以保持其在規定的恆定溫度下。對於理想氣體,分子體積 (v) 為零或沒有體積,並且它們不相互作用。現在,根據理想氣體定律,壓力 (p) 與溫度 (T) 和量 (q) 線性變化,但與體積 (v) 成反比,即**pV=nRT**,在這個方程式 (eq) 中,符號 R 是一個常數,稱為**普適氣體常數**,它對所有氣體 (g) 的值都相同。等溫過程 (p) 可以用理想氣體定律表示為**pV=常數 或 p1V1=p2V2**。
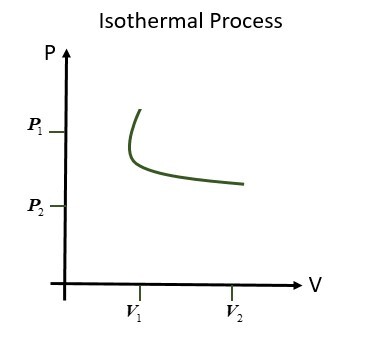
表示等溫過程的P-V圖
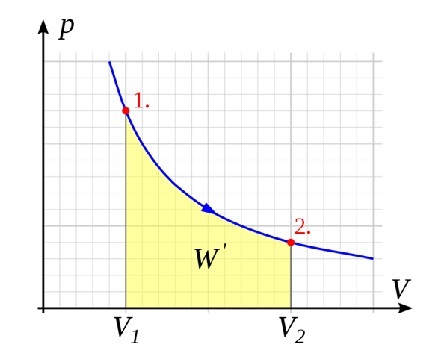
Zátonyi Sándor (ifj.), Fizped, Izoterm pV munka, CC BY 4.0
對於等溫過程,$\mathrm{pV=常數 或 p_1 V_1=p_2 V_2\: 或\: P\propto \frac{1}{V}}$。我們知道,對於等溫過程,溫度 (T) 保持不變。在 PV 圖中,如果壓力 (P) 和體積 (v) 的乘積保持恆定,即**pV=常數**,無論常數值是多少,該過程都表示為等溫過程。常數值完全取決於溫度 (T),但如果溫度 (T) 保持恆定,則它保持不變 (c)。
定義等溫膨脹的方程
對於等溫過程,當系統的內能**(ΔU)**發生變化時,則由以下條件表示:
$$ΔU=q+w ....(1)$$
其中 ΔU 表示內能的變化,q 表示系統釋放的熱量,w 表示對系統所做的功。
$$\mathrm{ΔU=q+p_{ex} ΔV}$$
由於$\mathrm{w (做功) = p_{ex} ΔV}$,這是在真空條件下所做的功。因此,方程-(1)也可以寫成這種形式。現在,讓我們以氦氣 (He) 等理想氣體為例,在真空 (v) 的存在 (p) 下進行等溫膨脹 (e)。因此,在這種真空情況下所做的功 (W.D) 將為零或空,即 w=0 或 p_ex=0。因此,根據焦耳的實驗 (e),q=0,因此可以得出結論,所做的功 (W.D.) 為零 (即) ΔU=0。
例子
一些等溫過程的例子如下:
藉助熔化 (m) 和蒸發 (e) 過程 (p) 對不同液體 (l) 的狀態或相進行的改變是等溫過程 (p) 的例子。
該過程或等溫過程 (p) 的工業 (i) 應用的一個例子 (e) 是**卡諾發動機**。在這個特殊的發動機中,一些部件是等溫地取出的。
冰箱也遵循這個概念。冰箱工作中發生的一系列變化,但內部溫度 (T) 保持恆定。
**熱泵**是另一個基於等溫過程的例子。
等溫過程和絕熱過程的區別
| 等溫過程 | 絕熱過程 |
|---|---|
| 發生熱傳遞。 | 此過程中沒有熱傳遞。 |
| 在這個過程中,對於任何給定的體積 (v),根據理想氣體方程,壓力 (p) 更高。 | 在這個過程中,在給定的體積 (v) 下,壓力 (p) 更低。 |
| 在這個過程中,用 T 表示的溫度保持恆定。 | 在這個過程中,由於系統內能 (e) 的變化,溫度 (T) 會發生變化。 |
| 從系統 (s) 附近存在的熱庫 (t) 中,可以向系統 (s) 新增或移除 (取出) 熱量 (H) 以保持溫度恆定。 | 這裡,熱量 (H) 沒有變化,因此沒有新增 (add) 或減去 (subs) 熱量。 |
| 緩慢的轉換過程。 | 快速的轉換過程。 |
結論
在熱力學(化學的一個分支)中,等溫過程 (p) 是一種熱力學過程,其中系統的溫度 (T) 保持恆定 (c),即 ΔT=0。這種過程通常發生在系統與外部熱庫接觸,並且系統變化足夠緩慢,允許系統透過熱量 (ΔH) 交換持續調整到熱庫的溫度 (T)。對於理想氣體,分子或原子之間所有的碰撞都是完全彈性,理想氣體中不存在分子間的吸引力,因為理想氣體分子運動速度很快,並且彼此相距很遠,因此它們不會相互作用。因此,它們可以在恆溫下輕鬆膨脹。
常見問題
1. 熱庫是什麼意思?
熱庫是一種熱力學系統型別,其熱容**(ΔC)**非常大,以至於當新增或提取相當數量的熱量時,熱庫的溫度 (T) 變化很小。
2. 完全彈性碰撞是什麼意思?
在完全彈性碰撞中,動能 (K.E.) 沒有淨轉化為其他形式的能量。
3. 寫出理想氣體定律方程。
理想氣體定律方程為:**pV=nRT**,其中 p=壓力,v=體積,n=摩爾數,R=氣體常數,T=溫度。
4. 提到等溫過程的兩個用途。
它用於卡諾迴圈。
它也用於熱泵。
5. 什麼是絕熱過程?
它被描述為系統 (s) 與周圍環境之間沒有熱傳遞的過程。


 資料結構
資料結構 網路
網路 關係資料庫管理系統(RDBMS)
關係資料庫管理系統(RDBMS) 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C語言程式設計
C語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP