純淨物與混合物的區別
簡介
純淨物是指不能被進一步分解的元素,例如氧氣、金屬和非金屬等。相反,混合物是兩種或多種元素混合在一起形成的,例如檸檬水。
我們不應該混淆純淨物和混合物。它們是兩個獨立的實體。純淨物是純元素,不能被進一步分解成更小的實體。它們可以存在於任何物質狀態,例如液體、固體或氣體。混合物是兩種或多種元素或物質的組合,可以透過一個簡單的例子理解。水是由兩個元素氫和氧組成的水分子,氫和氧是兩個獨立的元素,它們是純淨物。當它們透過化學鍵結合時,就會形成水,即化合物。當我們製作檸檬水時,我們會將水、糖、鹽和檸檬混合在一起。這種檸檬水是糖、水、鹽和檸檬的混合物。因此,混合物是一些純元素的混合物或組合,它們是混合的,而不是透過任何化學鍵結合的。
什麼是純淨物?
純淨物是指不能分解成更小部分的元素或單個實體。例如金屬和非金屬。它們是由兩種相同的元素形成的,例如氧氣分子、氫氣分子、金、銀、鐵等,即使將金條折斷,它仍然是金。
純淨物可以以任何一種形式存在,例如液體、固體或氣體。具有不同分子排列的純淨物在所有階段的所有相中都保持不變。例如:碳分子是一種純淨物,存在於石墨、金剛石和氣體等不同形式中。即使在高壓下,它們在不同相中也保持恆定。
純淨物只包含一種型別的原子或元素。它們是均一的。水也被認為是純淨物。冰是均一的,以固體形式存在,類似地,水蒸氣形式以氣體形式存在。
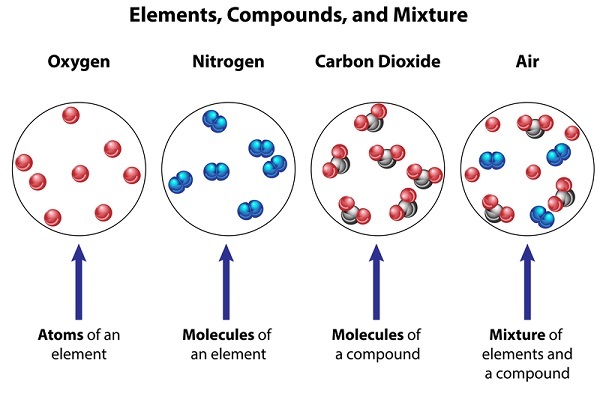
純淨物的型別
根據純淨物的化學組成,可以將其分為兩部分。
元素 - 元素是自然界中以金屬、非金屬和準金屬形式存在的純淨物。它們不能透過任何化學或物理變化分解成更簡單的形式。它們是純淨且均一的。它們具有較高的熔點和沸點。
例子 - 金、銀、銅、氫、氧、鐵、鋁、硫、金剛石等。
化合物 - 化合物是由兩種或多種金屬或元素透過化學鍵結合形成的。它們也是均一的,因為它們以固定比例由兩種或多種純元素組成。它們不能透過物理方法分離,但可以透過其他化學或電化學方法分離。它們表現出與其組成的元素不同的性質。它們具有較高的熔點和沸點。它們透過離子鍵或共價鍵結合。
例子 - 水分子、氨、食鹽、小蘇打等。
例子
元素是存在於元素週期表中的金屬、非金屬或準金屬。化合物是這些元素化學反應形成的產物。以下是純淨物的一些例子。
| 元素 | 化合物 |
|---|---|
| 金屬 - 鐵 $\mathrm{(Fe)}$、銀 $\mathrm{(Ag)}$、金 $\mathrm{(Au)}$、銅 $\mathrm{(Cu)}$、鈉 $\mathrm{(Na)}$、鋰 $\mathrm{(Li)}$、鉀 $\mathrm{(K)}$、鎂 $\mathrm{(Mg)}$、鈣 $\mathrm{(Ca)}$ 等。 | 水分子 $\mathrm{(H_{2}O)}$、二氧化碳 $\mathrm{(CO_{2})}$、氨 $\mathrm{(NH_{4})}$、過氧化氫 $\mathrm{(H_{2}O_{2})}$、食鹽 $\mathrm{(NaCl)}$、酒精 $\mathrm{C_{2}H_{5}OH}$、硫酸 $\mathrm{H_{2}SO_{4}}$ 等。 |
| 非金屬 - 氫 $\mathrm{(H)}$、氦、氧 $\mathrm{(O)}$、碳 $\mathrm{(C)}$、硫 $\mathrm{S}$、氯 $\mathrm{(Cl)}$、溴 $\mathrm{(Br)}$ 等。 | 其他例子還有小蘇打 $\mathrm{(NHCO_{3})}$、我們使用的藥物如阿司匹林等。 |
| 準金屬 - 銻 $\mathrm{(Sb)}$、硼 $\mathrm{(B)}$、鍺 $\mathrm{(Ge)}$、砷 $\mathrm{(As)}$ 等。 | 碳水化合物如葡萄糖 $\mathrm{(C_{6}H_{12}O_{6})}$、蔗糖和蛋白質分子如白蛋白、組蛋白、球蛋白等。 |
什麼是混合物?
混合物是由兩種或多種混合在一起的物質組成的。它們沒有化學鍵結合在一起。混合物可以透過物理或化學方法分離,例如分離漏斗、蒸餾法等。如果元素或物質以不同的比例混合,則混合物可以是均一的或非均一的。混合物的製備不消耗能量。它們表現出與其組成的元素相同的性質。
混合物的型別
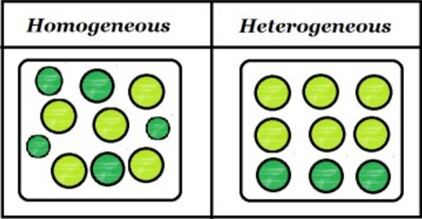
混合物有兩種型別 - 均一混合物和非均一混合物。讓我們瞭解更多資訊。
均一混合物 - 兩種溶質或溶劑均勻混合在一起,肉眼無法分辨的混合物稱為均一混合物。
例如牛奶和水、糖和水、空氣、墨水、鋼、青銅金屬、鹽在水或溶劑中、果汁、冰淇淋等。
非均一混合物 - 混合物中兩種組分混合不均勻。它們肉眼可見。
例如沙子在水中和油在水中、懸浮液、我們的血液。它們形成膠體溶液並表現出丁達爾效應。
例子
我們在日常生活中使用的混合物例子很多,下面列舉了一些。
| 均一混合物 | 非均一混合物 |
|---|---|
|
|
純淨物與混合物的區別
我們已經瞭解了純淨物和混合物是什麼,它們彼此之間存在很大差異。讓我們看看純淨物和混合物的區別。
| 純淨物 | 混合物 |
|---|---|
| 純淨物由相同的元素組成。 | 混合物由兩種或多種不同的元素或化合物組成。 |
| 它們是均一的。 | 它們既可以是均一的,也可以是非均一的。 |
| 它們表現出相同元素的性質,但在化合物中,它們表現出與元素不同的性質。 | |
| 它們表現出與其形成的元素的性質。 | |
| 它們是純淨的 | 它們是不純的,因為它們由多種成分組成。 |
| 它們不能透過物理或化學方法分解成更小的量。 | 它們可以透過物理或化學方法分離成元素。 |
| 例子 - 金屬、非金屬、準金屬、空氣、水等。 | 例子 - 煙霧、膠體溶液、懸浮液、飲料、漂白劑等。 |
結論
在本教程中,我們學習了純淨物和混合物。我們瞭解到,純淨物是純元素或純元素的混合物,而混合物是由兩種或多種元素或物質混合形成的。這些物質分為元素和化合物。元素是純淨的物質,主要存在於元素週期表中,而化合物則透過共價鍵或離子鍵結合在一起。它們具有與其組成的元素不同的性質,但元素具有相同的性質,因為它們是純淨物。另一方面,混合物分為均一混合物和非均一混合物,可以透過化學或物理方法分離。
常見問題
1. 什麼是膠體溶液?
膠體溶液是一種非均一混合物,其中溶質的粒子分散在溶液中。這些粒子肉眼不可見。膠體溶液有兩個階段:分散相和分散介質。例如氣溶膠、泡沫、乳液、凝膠等。
2. 什麼是丁達爾效應?
當一束光穿過膠體溶液時,光會被粒子散射。這種散射可以透過光的路徑觀察到。膠體粒子對光的散射稱為丁達爾效應。
3. 什麼是懸浮液及其用途?
懸浮液是一種異質混合物,顆粒尺寸相當大,例如 100 mm,它們懸浮在整個混合物中。如果懸浮液靜置,溶質的顆粒會沉降到溶液底部。它們用於製備一些藥物,如氫氧化鎂乳劑、止咳糖漿、油漆、粉刷等。
4. 人體血液是混合物還是化合物?
人體血液是蛋白質、血漿、紅細胞、白細胞和血小板的異質混合物。血漿是液體部分,由鹽和水組成,固體部分是紅細胞和白細胞。它們可以透過離心法分離。所以血液是混合物,而不是化合物。
5. 給出一些非金屬元素的例子?
非金屬不具有延展性,也不是良好的導體。一些非金屬元素的例子包括氧、氫、氯、溴、磷、硒、碘等。


 資料結構
資料結構 網路
網路 關係資料庫管理系統
關係資料庫管理系統 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C 語言程式設計
C 語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP