分子與化合物之間的區別
簡介
分子和化合物之間存在著重大的區別,每個人都應該瞭解。當化學鍵連線任意兩個或多個原子時,就會形成分子。而化合物是由不同化學元素的不同原子組成的分子。所有化合物都是分子,但並非所有分子都是化合物。分子僅僅是任何原子的組合。但是,當原子組合不同於元素時,就被稱為化合物。氫氣 (H2) 和氧氣 (O2) 都是分子,因為它們包含兩個或多個原子。而碳酸鈣 (CaCO3)、NaCl 和 H2O 被歸類為化合物,因為它們包含不同的成分。
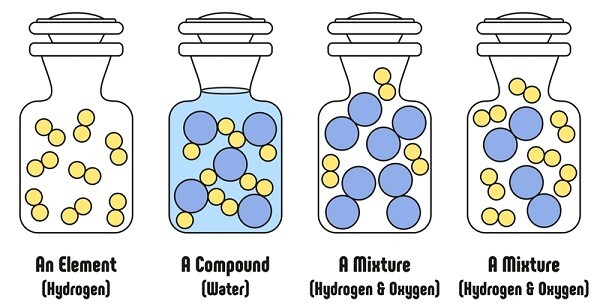
什麼是分子?
它是構成化學元素的成分的最小粒子,其特性與元素的特性基本相同。它們由透過重要的化學鍵結合在一起的原子組成。這種鍵可能是電價鍵,即透過共享電子形成,也可能是共價鍵,即透過交換電子形成。它們與離子的區別在於它們的性質是中性的,這意味著它們既沒有正 (+) 電荷,也沒有負 (-) 電荷。它們僅僅由 2 個原子的反應產生。例如,N2、O2 和 H2。
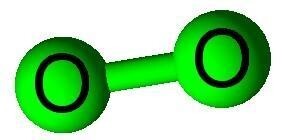
同核與異核
| 同核雙原子分子 | 異核雙原子分子 |
|---|---|
| 它們由兩個透過共價鍵結合在一起的相同化學元素的原子組成。 | 它們是由兩個不同化學元素的兩個原子透過共價鍵結合在一起形成的化合物。 |
| 穩定同位素非常穩定,但不會發生放射性衰變。 | 它們具有不同化學元素的原子。 |
| 它們具有非極性共價鍵。 | 它們具有極性共價鍵。 |
| 它們具有相同的原子。 | 它們具有不同的原子。 |
化合物的定義
它們是由來自不同元素的原子的化學鍵合產生的化學化合物。這些不同的原子各自具有不同的電荷;帶正 (+) 電荷的(原子)是電子虧損的,而帶負 (-) 電荷的(原子)是電子富裕的。透過結合在一起從而生成新的分子,這兩個不同的原子結合在一起以達到中性。例如,帶正電荷的氫原子 H+ 和帶負電荷的氧 (O) 原子以比例質量化學結合形成水 (H2O)。因此,水是一種化合物,因為它是由兩種不同的元素,氫和氧的結合產生的。二氧化碳也是化合物的一個例子。
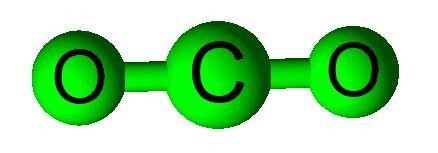
化學式
它們以它們的化學式來區分。化學式詳細說明了構成特定化學化合物的原子碎片。水的化學式為 H2O,表示兩個氫原子和一個氧原子結合形成一個 H2O。食鹽的化學式為氯化鈉 (NaCl),這表明一個鈉 (Na) 原子和一個氯 (Cl) 原子結合形成一個氯化鈉 (NaCl)。
化合物的型別
根據它們的來源,它們被分為兩類。
無機化合物 - 它們通常從非生物來源(如岩石和礦物)中獲得。例如,食鹽、大理石、蘇打、小蘇打、二氧化碳、氨、硫酸等
有機化合物 - “有機”一詞指的是生物體中發現的各種器官。有機化合物是由活生物體(如植物和動物)形成的。碳 (C) 已被確定為所有有機分子中的重要組成部分。它們通常被稱為碳 (C) 化合物。例如,甲烷、乙烷、丙烷、酒精、醋酸、糖、蛋白質、油脂、脂類等
根據它們的特性,它們被分為三類。
酸 是酸性的化學化合物,它們與水 (H2O) 反應,使藍色石蕊試紙變紅。例如,硫酸 (H2SO4)、乳酸 (C3H6O3)、鹽酸 (HCl)、檸檬酸 (C6H6O7)、碳酸 (H2CO3)、硝酸 (HNO3) 等。
鹼 是苦味的化學化合物,它們與水 (H2O) 反應,使紅色石蕊試紙變藍。例如,氫氧化鈣 Ca(OH)2、氫氧化鎂 Mg(OH)2、氫氧化鈉 (NaOH) 等。
鹽 由酸和鹼的相互作用形成。例如,氯化鈉 (NaCl)、氯化鈣 (CaCl2)、硝酸鈣、硫酸鋅等。
化合物的例子
NaCl(鹽)
H2O2(過氧化氫)
C2H6O(酒精)
CH4(甲烷)
C55H72O5N4Mg(葉綠素)
一些常用化合物的例子及其分子式
| 俗名 | 化學化合物 | 化學式 |
|---|---|---|
| 瀉鹽 | 七水硫酸鎂 | MgSO4·7H2O |
| 漂白水/次氯酸鈉 | 次氯酸鈉 | NaOCl/NaClO |
| 漂白粉 | 氯氧化鈣 | CaOCl2 |
| 乾冰 | 固體二氧化碳 | CO2 |
| 苛性鉀 | 氫氧化鉀 | KOH |
| 氯仿 | 三氯甲烷 | CHCl3 |
| 酒石酸氫鉀 | 酒石酸氫鉀/酒石酸鉀 | KC4H5O6 |
| 白雲石 | 碳酸鈣鎂 | CaMg(CO3)2 |
| 甘汞 | 氯化亞汞 | Hg2Cl2 |
| 硼砂 | 十水四硼酸鈉/硼酸鈉 | Na2B4O7·10H2O |
| 芒硝 | 十水硫酸鈉 | Na2SO4·10H2O |
| 甘油 | 丙三醇 | C3H8O3 |
| 石膏 | 二水硫酸鈣 | CaSO4·2H2O |
| 小蘇打 | 碳酸氫鈉或碳酸氫鈉 | NaHCO3 |
分子和化合物的區別
| 分子 | 化合物 |
|---|---|
| 它們由兩個或多個透過化學鍵連線的原子組成。 | 它們由兩個或多個透過化學鍵結合的不同元素組成。 |
| 它們可能是異核的,也可能是同核的。 | 它們由多種成分組成。 |
| 可能易揮發。 | 由於它們處於物理形態,因此它們始終穩定。 |
| 共價鍵或離子鍵 | 離子鍵、金屬鍵或共價鍵 |
| 並非所有分子都是化合物。 | 所有化合物都是分子。 |
| 肉眼不可見 | 肉眼易見 |
| 一組透過強大的力量結合在一起的原子 | 整體的真實物質 |
結論
因此,很明顯分子和化合物是如何相關的,儘管兩者都具有不同的特徵,包括基於其成分以及原子的特徵。每個分子的質量根據其形成的原子而有所不同,因此每個化合物的質量也不同。除了質量之外,其他性質如硬度、顏色、狀態等都依賴於原子,因為原子是分子和化合物都依賴的基本單位。水、甲烷以及溫室氣體都是既是分子又是化合物的例子。
常見問題
1. 分子的不同種類有哪些?
單原子分子是指僅包含一個元素的原子的分子。例如,Na、He 等。雙原子分子是指在一個元素的分子中具有兩個原子的分子。例如,O2 和 N2。多原子分子是指在一個元素的分子中具有兩個以上原子的分子。例如,P4、S8 等。
2. 分享一些分子的例項。
臭氧、氧分子和氮都是分子的例子。
3. 根據其鍵,化合物的 3 種類型是什麼?
離子化合物、共價化合物和配位化合物是 3 種類型的化合物。
4. 分子是否可以只有一個原子?
它被定義為透過化學鍵結合在一起的兩個或多個原子的電中性集合。因此,根據定義,分子不能由單個原子產生。
5. 當原子結合形成分子時,會發生什麼?
當原子結合形成分子時,化學鍵將它們結合在一起。這些鍵是在原子共享或交換電子時形成的。只有最外層殼層的電子具有結合活性。


 資料結構
資料結構 網路
網路 關係型資料庫管理系統
關係型資料庫管理系統 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C 語言程式設計
C 語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP