固體的特性
簡介
固體是緊密堆積的結構,不容易受外部因素的影響。
它們具有確定的體積、質量和形狀。然而,固體不會流動。固體的化學和物理性質在固態化學和固態物理學中進行研究。
自然界有四種不同的物質狀態。根據它們的分子間相互作用以及組成粒子的性質,它們被分類為固體、氣體、液體和等離子體。
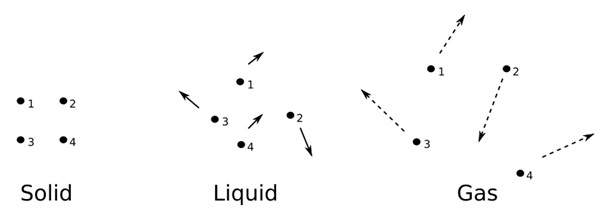
Solid-liquid-gas.jpg: Sadi Carnot衍生作品: Dave.Dunford (talk) 13:43, 15 December 2010 (UTC), Solid-liquid-gas,標記為公共領域,維基共享資源上有更多詳細資訊
什麼是固態?
固體是三種物質形態之一,具有緊密堆積的結構以及確定的體積和形狀。
化學鍵將分子結合在一起,這是堅硬結構的原因,因為分子牢固地結合在一起,它們的動能小於氣體和液體。
此特性使它們能夠抵抗外部因素的作用,因此保持恆定的體積和形狀,這與易揮發的氣體和液體相反。
固體的特性
由於顯著的分子間相互作用將物質的組成粒子結合在一起,因此固體具有特定的重量、體積和形狀。在低溫下,分子間力趨於控制熱能,固體保持穩定狀態。對於給定的物質,液體和固態的體積和質量相同。
導電性、密度和光學透射只是固體的眾多特性中的一部分。
常見的食鹽、水冰、乾冰、岩石、大多數金屬和木材都是固體的例子。當固體被加熱時,原子或分子會獲得動能。
固體有兩種型別:晶體和非晶體。最常見的固體形式是晶體固體。它們的特徵是原子以一致的晶體排列,賦予其長程有序性。非晶體或無定形物質則缺乏這種長程有序性。晶體固體是指原子、離子或分子以規則、明確的模式排列的固體。
分子固體、離子固體、共價固體和金屬固體是四種主要的固體型別。離子固體由帶正電和負電的離子組成,這些離子透過靜電相互作用結合在一起;鍵合強度以晶格能表示。離子固體具有高熔點且非常堅硬。
某些化學物質會形成晶體固體,其粒子以高度有序的方式排列;而另一些則形成非晶固體,其內部結構無序。
固體的機械效能解釋了諸如變形和抗力之類的特性。塑性、磨蝕性、延展性、展性以及韌性都是機械效能的例子。
固體的特點是其結構剛度和抗力,能夠抵抗施加在其表面的力。與液體不同,固體物質不會移動以適應容器的形狀,也不會像氣體一樣膨脹以充滿所有可用空間。
固體具有確定的形狀和尺寸,並且不可壓縮。
晶體材料中的離子、原子或分子以有序且對稱的方式排列,這種排列在整個晶體中重複出現。晶胞代表固體中最小的重複結構,類似於牆上的磚塊。晶格是由晶胞組成的網路。
用途
固態材料廣泛應用於我們周圍的各個地方。其中最重要的包括:
行動電話和個人電腦是電子裝置的例子。
雷射器和光纖是光學裝置的例子。
因此,整個現代發明概念都基於固態物理學的概念。
應用
諸如建築物中的電線和窗玻璃,以及冰箱中的磁鐵等常見物品都嚴重依賴於固態。
邏輯和儲存位由固態矽製成。
結論
可以得出結論,固體是四種物質狀態之一,具有緊密堆積的結構。固體的特點是其體積和形狀。固體不可壓縮,因此不會流動。強烈的分子間相互作用將組成粒子結合在固體中。根據組成粒子的排列方式,固體分為晶體/非晶體兩類。晶體固體具有規則的幾何形狀、各向異性的熔點和鋒利的邊緣。它們具有明確的熔化熱和解理特性。非晶態材料是無序的偽液體或過冷液體。它們沒有解理特性,並且是各向同性的。它們在較寬的溫度範圍內軟化,並且在加熱時可能會結晶。
常見問題
Q1. 為什麼糖比空氣和水更堅硬?
A1. 糖是一種晶體固體,其組成分子在三維空間中緊密堆積。
在這個三維區域中,它們透過強大的分子間力緊密結合在一起,這些力在長距離內以可預測的模式作用。這限制了這些分子的移動性,使它們只能在其平均位置附近振動。另一方面,在液體和氣體中,分子由中等和弱的分子間力結合在一起。因此,它們具有動能並且可以移動。因此,它們不如糖堅硬。
Q2. 玻璃是一種固體。為什麼它被稱為過冷液體?
A2. 玻璃是非晶固體,因為它們缺乏明確的形狀,並且由透過相對較弱的力結合在一起的分子組成。雖然它們具有規則的重複模式,但這些模式只能在有限的距離內觀察到。因此,粒子的結構變得極其無序。由於組成粒子的無序排列,它們被稱為偽固體或過冷液體。
Q3. 為什麼石墨比金剛石更能導電?
A3. 要導電,化合物必須包含自由電子或離域電子。在石墨中,每個碳原子與附近的三個其他碳原子相連。這釋放了第四個電子使其能夠移動。另一方面,金剛石由於其由強共價鍵形成的四面體結構,不包含自由電子。由於這些自由電子,石墨與不含自由電子的金剛石相比,能夠導電。
Q4. 塑膠是各向同性材料嗎?
A4. 各向同性材料的特性在不同方向上測試時不會發生變化。塑膠是一種非晶固體,由於組成粒子的無序排列,其特性在不同方向上不會改變。它非常延展,可以形成任何形狀。由於其組分的特性在任何方向上都是相同的,因此其行為也高度可預測。所有這些特性共同使其成為各向同性的。
Q5. 為什麼石墨比金剛石更脆?
A5. 金剛石和石墨都是碳化合物。區分它們的是組成粒子鍵合的性質。在金剛石中,碳原子透過強共價鍵緊密地結合在晶格結構中。在這個四面體結構中,每個碳原子都與另外 4 個碳原子相連,並且沒有自由電子。因此,金剛石更堅硬。在石墨中,碳原子的結合形成了自由電子。每個碳原子只與附近的三個其他碳原子相連。由於其特性,石墨比金剛石更脆。


 資料結構
資料結構 網路
網路 關係型資料庫管理系統 (RDBMS)
關係型資料庫管理系統 (RDBMS) 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C語言程式設計
C語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP