碳酸氫鹽
簡介
在碳酸脫質子的過程中,會形成一箇中間多原子陰離子。這個陰離子稱為碳酸氫根陰離子,其化學式為$\mathrm{HCO_{3}^{-}}$。碳酸氫鹽這一術語由英國化學家威廉·海德·沃拉斯頓於1814年提出。在IUPAC命名法中,碳酸氫根離子也稱為氫碳酸根。作為陰離子,碳酸氫根帶負電荷,是一種兩性分子。兩性物質是指既能與酸反應又能與鹼反應,並同時具有酸性和鹼性的物質。碳酸氫根的結構類似於硝酸,這解釋了碳酸氫根與硝酸的等電子性。
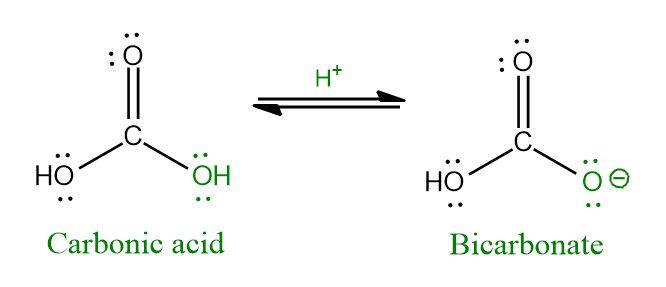
碳酸氫根陰離子和碳酸之間的結構關係
碳酸氫根離子的結構由一箇中心碳原子組成,周圍以三角平面幾何構型排列著一個氧原子、一個氧離子以及一個羥基。另一方面,碳酸的結構具有相同的三角平面幾何構型,但它有兩個羥基和一個透過雙鍵連線的氧原子。碳酸氫根的共軛酸是碳酸根離子,而其共軛鹼是碳酸。因此,碳酸和碳酸氫根陰離子可以透過消除或新增氫原子相互轉換。
碳酸氫鹽的應用
碳酸氫根離子的最重要應用之一包括透過碳酸氫鹽緩衝系統調節二氧化碳。該系統中碳酸氫鹽的功能是維持細胞外二氧化碳。碳酸氫鹽緩衝系統是主要的細胞外緩衝系統。組織代謝過程中產生的二氧化碳由碳酸氫鹽緩衝系統移除。碳酸氫根離子在此過程中充當質子受體,而碳酸則充當質子供體。碳酸氫鹽系統可以改變血液的pH值。
$$\mathrm{H_{2}CO_{3}+H_{2}O\rightleftharpoons HCO_{3}^{-}+H^{+}}$$
各種碳酸氫鹽的應用不僅取決於陰離子,還取決於構成化合物的陽離子。
碳酸氫鈉
碳酸氫鈉,也稱為碳酸氫鈉,是許多美味佳餚的重要成分。俗稱小蘇打、蘇打粉或碳酸氫鈉,是一種無機鹽,用途廣泛。碳酸氫鈉最早由法國化學家尼古拉·勒布朗於1791年在實驗室合成。它可以從天然礦物鈉鹼(nahcolite)或熱鉀鹽(thermokalite)中提取。碳酸氫鈉的天然十水合物被稱為天然鹼(natron)。小蘇打的化學式為$\mathrm{NaHCO_{3}}$。
合成
碳酸氫鈉的工業合成涉及碳酸鈉與二氧化碳和水的反應。該反應生成碳酸氫鈉白色固體沉澱。
$$\mathrm{Na_{2}CO_{3}+CO_{2}+H_{2}O\to 2NaHCO_{3}}$$
另一種製備方法包括在水存在下,氯化鈉、氨和二氧化碳的反應。這被稱為索爾維法。
$$\mathrm{NH_{3}+H_{2}O+CO_{2}\to NH_{4}HCO_{3}}$$
$$\mathrm{NH_{4}HCO_{3}+NaCl\to NaHCO_{3}+NH_{4}Cl}$$
碳酸氫鈉的性質
碳酸氫鈉的性質如下:
它是白色結晶固體。
熔點為50攝氏度。
沸點為851攝氏度。
易溶於甲醇和丙酮。
不溶於乙醇。
摩爾質量為84克/摩爾。
在水中呈鹼性,是一種弱鹼。
$$\mathrm{NaHCO_{3}+H_{2}O\to H_{2}CO_{3}+NaOH}$$
pH值為8.31。
它是一種兩性化合物。
$$\mathrm{NaHCO_{3}+HCl\to H_{2}CO_{3}+NaCl}$$
$$\mathrm{NaHCO_{3}+NaOH\to Na_{2}CO_{3}+H_{2}O}$$
在大約80-100攝氏度下發生熱分解。
$$\mathrm{2NaHCO_{3}\to Na_{2}CO_{3}+H_{2}O+CO_{2}}$$
微溶於水。
碳酸氫鈉的應用
碳酸氫鈉在烹飪、煙火、農業、製藥、醫學等領域有著廣泛的應用。其中一些應用如下:
在烹飪和烘焙中,碳酸氫鈉用作膨鬆劑(或發酵劑)。它通常與酸性物質一起使用,以觸發產生二氧化碳的反應。
它是煙花成分的主要組成部分。
它用於降低燃燒反應的速率。
它可用作消毒劑。
它用作滅火器。
碳酸氫鉀
與碳酸氫鈉一樣,碳酸氫鉀也是一種重要的商業化合物。碳酸氫鉀是由陽離子鉀離子和陰離子碳酸氫根離子組成的無機鹽。根據IUPAC命名法,它被稱為碳酸氫鉀。碳酸氫鈉和碳酸氫鉀曾經都被稱為蘇打,意思是充氣鹽。碳酸氫鉀的化學式為$\mathrm{KHCO_{3}}$。
碳酸氫鉀的性質
其中一些性質如下:
它是白色固體。
可以以粉末狀和結晶狀存在。
呈鹼性。
摩爾質量為100.115克/摩爾。
它不沸騰,在120攝氏度分解。
熔點為292攝氏度。
它是一種弱鹼。
pH值為8.2。
易溶於水。
不溶於乙醇。
無味。
它是兩性的。
合成
碳酸氫鉀的製造過程涉及碳酸鉀水溶液與二氧化碳的反應。
$$\mathrm{K_{2}CO_{3}+H_{2}O+CO_{2}\to 2KHCO_{3}}$$
該反應生成的碳酸氫鉀會分解以合成高純度的碳酸鉀。
$$\mathrm{2KHCO_{3}\to K_{2}CO_{3}+CO_{2}+H_{2}O}$$
碳酸氫鉀的應用
碳酸氫鉀的應用與碳酸氫鈉相似。
由於它是良好的二氧化碳來源,因此它被用作烘焙、烹飪和飲料中的膨鬆劑。
它用於調節藥物中的pH值。
它用作葡萄酒生產中的新增劑。
它用於滅火器。
它用於中和農業中的酸性土壤。
結論
總而言之,碳酸氫鹽是廣泛使用的無機化合物。這些化合物參與許多代謝功能,如呼吸、排洩、調節等。這些化合物的無毒性使其非常適合生產烘焙和烹飪食品。不僅用於烹飪,它們還可用作家庭和工業中的清潔劑和除臭劑。像可樂這樣的冷飲含有碳酸氫鹽以產生起泡效果。碳酸氫鉀通常用於生產低鈉食品。碳酸氫鹽的鹼性在各種藥物緩衝液中得到利用。碳酸氫鹽的生產通常以其各自的碳酸鹽為底物。
常見問題
問1:碳酸氫鈉的結構是什麼?
答:碳酸氫鈉的結構如下所示

問2:碳酸氫鉀的結構是什麼?
答:碳酸氫鉀的結構如下所示

問3:哪種碳酸氫鹽用於抗酸劑?
答:碳酸氫鈉用於抗酸劑。它與胃酸反應產生二氧化碳,可以治療消化不良。
問4:蘇打和蘇打粉有什麼區別?
答:蘇打是碳酸鈉 ($\mathrm{Na_{2}CO_{3}}$),蘇打粉是碳酸氫鈉 ($\mathrm{NaHCO_{3}}$)。
問5:為什麼鹼土金屬(第二族)碳酸氫鹽在水中微溶?
答:鹼土金屬(第二族)碳酸氫鹽在水中微溶是因為它們的晶格能很高。


 資料結構
資料結構 網路
網路 關係資料庫管理系統 (RDBMS)
關係資料庫管理系統 (RDBMS) 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C語言程式設計
C語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP