惰性氣體的用途和應用
引言
瞭解惰性氣體在我們日常生活中的貢獻,對於理解化學中的一個重要方面——惰性氣體的用途和應用至關重要。惰性氣體表現為純非金屬化合物,它們是無色無味的低熔點和沸點的氣體。液態時,這些元素不是良好的導電體。
惰性氣體以氣態形式存在的前提條件是標準溫度和壓力。惰性氣體的通式被認為是$\mathrm{ns^2np^6}$。惰性氣體通常具有非常穩定的電子構型,這使得它們的反應速率非常低。
什麼是惰性氣體?
惰性氣體通常指元素週期表第18族元素。這些元素包括:氦 (He)、氖 (Ne)、氬 (Ar)、氪 (Kr)、氙 (Xe) 和氡 (Rn)。
惰性氣體必須保持在標準狀態的溫度下才能以氣態存在。惰性氣體具有非常穩定的電子構型,不易形成分子,因此這些元素以單原子形式存在。
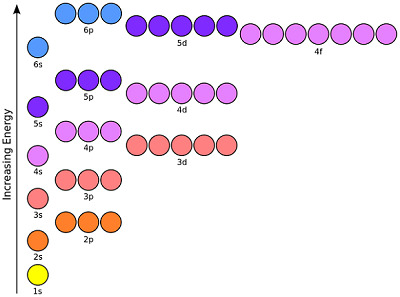
圖1:電子構型
CK-12 基金會,軌道表示圖,CC BY-SA 3.0
惰性氣體位於元素週期表的最右側,經國際純粹與應用化學聯合會 (IUPAC) 批准。該族包含非金屬元素。這些元素也以其成員命名,被稱為氖族或氦族。該族的所有元素都具有非常高的電離能。這些元素的電子在其最外層也均勻分佈。惰性氣體的密度隨著原子序數的增加而增加,導致惰性氣體元素的尺寸變大。
惰性氣體:性質
下面列出了所有惰性氣體的性質:
氦 (He) 的性質

圖2:氦的原子結構
氦也用其符號 He 表示,其原子序數為 2。在標準或正常條件下,氦 (He) 存在於無色單原子氣體中,本身沒有明顯的滋味。當使用少量氦 (He) 時,其作用方式無毒。它是其獨特族中的第一種氣體,也是所有氣體中最輕的。重要的是要知道,氦 (He) 是一種 s 區元素,其電子構型為 1s2。
氖 (Ne) 的性質
氖是一種化學元素,也用其符號 (Ne) 表示,氖 (Ne) 的原子序數為 10。標準溫度和壓力 (STP) 條件使氖 (Ne) 像其獨特惰性氣體族中的其他元素一樣保持無色單原子狀態。氖 (Ne) 是僅次於氦 (He) 的第二輕的惰性氣體。它位於第一週期,也屬於現代元素週期表第 18 族。
氬 (Ar) 的性質
氬 (Ar) 被認為是第三種惰性氣體,原子序數為 18。氬 (Ar) 通常是無色無味的,但在與電場接觸時會發出紫色或淡紫色的輝光。氬 (Ar) 的熔點約為 83.81K。
氪 (Kr) 的性質
氪 (Kr) 的原子序數為 36。它也屬於與前驅氬 (Ar) 相同的 P 族。其熔點約為 115.78K,其電子構型通常表示為 $\mathrm{[Kr]\: 4d^{10}5s^25p^6}$。
氙 (Xe) 的性質
第五種惰性氣體氙 (Xe) 的原子序數顯然是 54。其熔點已計算約為 161.4 K,其推導電子構型為 $\mathrm{[Xe]\:4f^{14}5d^{10}6s^26p^6}$。
氡 (Rn) 的性質
惰性氣體氡 (Rn) 的原子序數為 86。非常重要的是要指出,元素氡 (Rn) 本身具有放射性。氡 (Rn) 的熔點和沸點分別為 202K 和 211.5K,屬於元素週期表第六週期。
惰性氣體:發現
惰性氣體肉眼不可見,其非反應性使得它們很難被發現和觀察。1894 年,威廉·拉姆齊爵士進行了一項實驗來發現惰性氣體。他試圖去除空氣中的所有氣體,因此他加熱銅和鎂,並讓空氣透過它。觀察到,當使用 100cm3 空氣時,總是剩下 1cm3 空氣,這就是惰性氣體被發現的方式。
惰性氣體:用途和應用
冶金領域廣泛使用氬氣,以提供所需的惰性氣氛。鈦、鋁、不鏽鋼和鎂的焊接過程需要這樣的氣氛。它還在鈦的製造中經常使用。
鍺和矽晶體需要少量氬氣來生產電燈泡和電晶體。
氦在惰性氣體中具有最低的沸點,因此它用於雷射器以獲得較低的溫度。它在核反應堆中用作冷卻氣體。氦最常見的用途是填充飛艇和熱氣球。
氖用於放電管中以產生紅橙色輝光。
結論
惰性氣體通常是指元素週期表第 18 族元素。氦是所有氣體中最輕的,沸點也最低。由於其低導電性和放電特性,惰性氣體本質上是高度非金屬的,因此這些氣體在冶金領域得到廣泛應用。
常見問題
Q1. 惰性氣體能否以固體結構存在?
A1. 惰性氣體在冷卻或壓縮後可以以固態或液態存在。當其呈凝聚態時,可以稱為固態。
Q2. 氦氣會過期嗎?
A2. 惰性氣體氦氣不會過期或降低其質量。需要將其儲存在氣密性良好的鋼瓶中。
Q3. 吸入氖氣會有什麼後果?
A3. 氖氣是惰性的,但它被稱為單純性窒息劑。過量吸入會導致頭暈、噁心、嘔吐、意識喪失,甚至死亡。


 資料結構
資料結構 網路
網路 關係型資料庫管理系統 (RDBMS)
關係型資料庫管理系統 (RDBMS) 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C語言程式設計
C語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP