鈾
簡介
鈾於1841年由法國化學家歐仁·梅爾希奧·佩利戈首次分離出來。這種元素在19世紀被廣泛用於各種用途,例如使玻璃呈現出黃綠色調,也被稱為凡士林玻璃。1896年,科學家亨利·貝克勒爾首次發現了它的放射性。這一發現隨後在1934年由恩里科·費米進行了進一步研究。這項研究有助於發現由鈾同位素U-235引起的核裂變。
什麼是鈾?
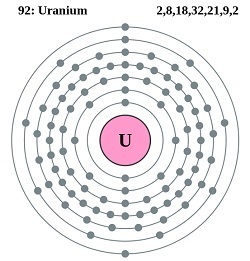
圖1:鈾的原子結構
Pumbaa(格雷格·羅布森的原創作品),電子層 092 鈾,CC BY-SA 2.0 UK
鈾是一種放射性元素,其性質並不十分強烈。鈾用U表示,其原子序數為92。它是一種重金屬,具有高度集中的能量來源。它是一種非常常見的元素,像錫和鎢一樣,存在於各種岩石中,濃度為2-4 ppm。它也存在於海水中。
鈾:發現
德國化學家馬丁·克拉普羅斯於1789年首次發現了鈾。他在檢查來自約阿希姆斯塔爾銀礦的瀝青鈾礦樣品時,發現了一種氧化鈾。該礦以前位於波希米亞,現在位於捷克。克拉普羅斯最初稱這種元素為鈾。這個名字的靈感來自於天王星。
鈾的化學性質
鈾的化學性質如下:
它屬於錒系元素。
它位於元素週期表第七週期和f區。
該元素的原子序數為92。
該分子的狀態在20°C時為固態。
鈾的電子構型為[Rn] 5f36d17s2。
它的ChemSpider ID為22425。這是一個免費的化學結構資料庫。
鈾的熔點和沸點分別為1135°C、2075°F、1408 K和4131°C、7468°F、4404 K。
該元素的密度為19.1 g cm−3。
它的相對原子質量為238.029。
234U、235U、238U是其主要的同位素。
鈾的CAS號為7440-61-1。
鈾的物理性質
鈾的物理性質如下:
純鈾的顏色為銀色,它在空氣中會迅速氧化。
天然鈾礦是其兩種同位素的混合物。U-238佔99.3%,其餘為U-235。
鈾是地球上最重的天然元素之一,這取決於原子核質量的增加。水的密度比鈾低18.7倍。
鈾有多種同位素,它們以不同的形式存在。
由於其高密度,它可用作飛機控制面的配重和輻射遮蔽。
大約66億年前,鈾首次在地球上形成。它在太陽系中並不常見,但它具有緩慢的放射性衰變,會產生熱量。這種熱量產生通常會導致大陸漂移和對流。
鈾:應用
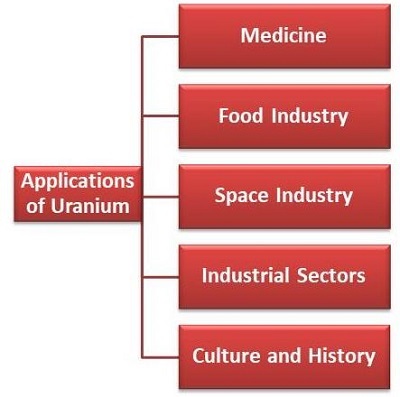
圖2:鈾的應用
鈾通常用作核電站發電的燃料。它還為世界提供了近14%的電力。其他主要用途如下:
醫學:它用作放射性元素,注入人體內以殺死特定器官中的癌細胞。
食品工業:它用於對容器進行滅菌,殺死害蟲、寄生蟲和細菌,從而使食物保持新鮮。
航天工業:宇航員在太空中遠離太陽,而鈾是產生熱量的絕佳替代品。
工業部門:鈾用於X射線、冶金、航空和汽車工業。
文化和歷史:該元素用於考古學中測量特定樣品的年齡。
鈾的影響
鈾的影響可以分為三個部分。
對礦工的影響
在鈾礦場作業的人們會直接接觸到鈾。為礦工採取的安全措施是基於其財務狀況的。它很少基於公共衛生福利。因此,礦場上的礦工直接暴露於影響其健康的放射性同位素。
對普通民眾的影響
鈾礦開採產生的危險廢物會汙染環境。即使沒有直接接觸,飲用危險廢水或吸入粉塵也會導致普通民眾患上各種致命疾病,包括癌症。
對環境的影響
鈾及其放射性同位素產生的熱量會導致大陸漂移。在尾礦上生長的植物會產生含有放射性物質的蔬菜。
結論
鈾富含放射性特性,因此對人體健康有害。鈾最初在戰爭中被用作核武器。然而,鈾也有一些有益的用途。它可以用作治療癌症的藥物,以及殺死細菌和害蟲的消毒劑。一些汽車公司發現,對於氨的生產,鈾比鐵更有效的催化劑。硝酸鈾用於照相顯影劑。鈾的化合價通常為+4或+6。
常見問題
問1. 鈾衰變需要多少年?
答:鈾經歷非常緩慢的放射性衰變。鈾同位素U-238的半衰期為45億年。
問2. 鈾何時變得安全?
答:鈾及其相關的衰變產物,如釷-230和鐳-226,將持續數千年具有危險性和放射性。然而,大約500年後,這些產物的放射性水平將降低。
問3. 鈾的膳食來源是什麼?
答:塊根類蔬菜,如土豆和甜菜,含有大量的鈾。牛肉、雞蛋、牛奶、貝類和魚類也含有鈾。
問4. 哪個地方的鈾產量最高?
答:哈薩克是全世界鈾產量最高的國家。2019年,其鈾產量佔全球的43%。在哈薩克之後,加拿大和南極洲的鈾產量最高。根據目前的用量,鈾還能使用80年。


 資料結構
資料結構 網路
網路 關係資料庫管理系統 (RDBMS)
關係資料庫管理系統 (RDBMS) 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C語言程式設計
C語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP