(a) 寫出鈉原子和氯原子的電子排布式。(b) 鈉原子和氯原子的最外層各有幾個電子?
(c) 透過電子轉移,說明NaCl由鈉原子和氯原子形成的過程。
(d) 為什麼氯化鈉的熔點很高?
(e) 電解精煉不純銅時,陽極和陰極分別是什麼?
(a) 下列原子的電子排布式為:
(i) 鈉 – 2, 8, 1
(ii) 氯 – 2, 8, 7
(b) 最外層電子數:
(i) 鈉 = 1
(ii) 氯 = 7
(c) 鈉原子和氯原子透過電子轉移形成NaCl的過程如下圖所示: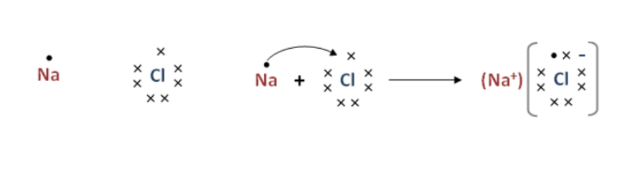

(d) 氯化鈉的熔點很高,因為它是一種離子化合物。離子化合物由帶電的離子組成,可以是正離子(陽離子)或負離子(陰離子)。離子間的吸引力非常強,難以破壞。因此,需要大量的能量才能破壞這些鍵。
(e) 銅的電解精煉過程中:
陽極: 厚塊的不純銅金屬
陰極: 薄片純銅金屬。

廣告

 資料結構
資料結構 網路
網路 關係資料庫管理系統(RDBMS)
關係資料庫管理系統(RDBMS) 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C語言程式設計
C語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP