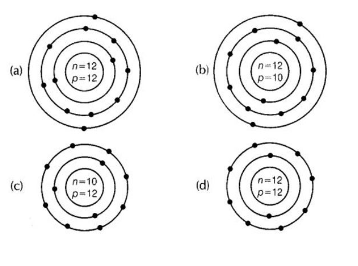
從圖 4.1 中識別 Mg2+ 離子,其中 n 和 p 分別表示中子和質子的數量。
 "
"
正確答案:(d)
解釋:鎂的原子序數 (Z) 為 12
質量數 (A) 為 24(因為 p = 12,n = A - Z = 24 - 12 = 12)。
Mg 原子的電子構型為 2, 8, 2。
Mg 2+離子的電子構型為 2, 8(正電荷是由於失去 2 個電子)。
鎂原子內部的質子和中子數量不受鎂原子形成鎂離子的影響。
選項 (B) 和選項 (C) 沒有正確表示中子 (n) 和質子 (p) 的數量。
選項 (A) 表示 Mg 原子,而不是 Mg 2+離子。

廣告

 資料結構
資料結構 網路
網路 關係型資料庫管理系統
關係型資料庫管理系統 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C 語言程式設計
C 語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP