氫氧化物
簡介
氫氧根是一種帶負電的二原子離子。它與帶正電的金屬(如鈉、鎂、鋁等)結合,也與乙基、甲基和芳香環等有機化合物結合。化合物的名稱由分子的字首或字尾表示。例如,當它與金屬鈉結合時,形成氫氧化鈉。當它與乙烷結合時,形成乙醇。
什麼是氫氧化物?
氫氧根離子是由氫原子和氧原子透過共價鍵結合形成的。它是一個帶負電的離子,也稱為羥基離子或氧化物陰離子。它在化學反應中充當鹼、催化劑、配體和親核試劑。它廣泛用於工業作為防腐劑、抗凝劑和鹼化劑。它是水分子的共軛鹼。它是最簡單的二元陰離子之一。它存在於自然界的多種礦石中,例如褐鐵礦、鋁土礦等。
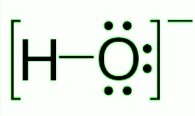
氫氧根離子
OH−和H+之間的關係是什麼?
在氫氧根離子中,氧的電負性比氫強。當它們形成共價鍵時,氧會將電子拉向自身,並在分子OH−上產生部分負電荷。這會吸引來自水或酸性介質中的正H+離子,形成水合氫離子。
當H+離子和氫氧根離子OH−的濃度相等時,它們形成水分子。它們相互吸引並形成水分子。
氫氧根離子的濃度決定溶液的pH值。
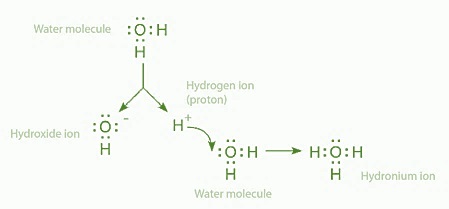
水合氫離子的形成
氫氧化鈉的化學式
氫氧化鈉是一種白色結晶固體。它的化學式是NaOH。它由鈉陽離子Na+和氫氧根陰離子OH−形成。它是一種廣泛用於工業和實驗室用途的鹼,例如清潔劑、制皂、炸藥、造紙工業等。它也稱為苛性鈉或燒鹼。
氫氧化鈉的結構
氫氧化鈉是由鈉離子和氫氧根離子透過離子鍵形成的。它是一箇中性分子,但它的單水合物形成正交晶體結構。其中,鈉被三個羥基離子和一個水分子包圍。
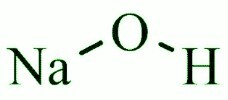
氫氧化鈉結構
氫氧化鈉的製備
氫氧化鈉可以透過多種方法制備,例如水銀電解法、氯鹼法、隔膜法或水銀電解法中的鹽水溶液。
透過鹽水電解法制備氫氧化鈉 - 在此過程中,鹽水,即NaCl溶液,在隔膜電池中進行電解。電池包含陰極和陽極。
水在陰極被還原,形成氫氣和氫氧根離子。
在陽極,鹽水NaCl分解成氯離子Cl−和鈉離子Na+。
在此過程中,氯氣和氫氣可能會結合並引起爆炸,因此為了避免它們的反應,陰極與石棉的多孔隔膜相結合。
之後,鈉和氫氧根結合形成氫氧化鈉。
氯氣和氫氣隨後被淨化並壓縮到氣瓶中。
在此反應中也會形成一些副產品,即鈉金屬,它在陰極被汞汞齊化。
在此過程中,溶液中產生的50%氫氧化鈉直接被去除,並進一步乾燥並以結晶形式NaOH·H₂O去除。
$$\mathrm{2H_{2}O\:2e^{-}\rightarrow\:H_{2}\:+\:2OH^{-}}$$
$$\mathrm{2Na\:+\:2OH^{-}\:\rightarrow\:2NaOH}$$
$$\mathrm{Na(aq)\:e^{-}\:+\:xHg(l)\rightarrow\:NaHg_{x}(l)}$$
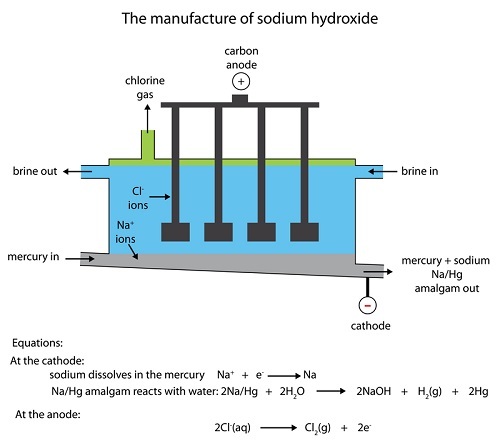
氫氧化鈉的製備
物理和化學性質
物理性質
| 物理性質 | 屬性 |
|---|---|
| 顏色 | 白色 |
| 外觀 | 結晶狀 |
| 化學式 | $\mathrm{NaOH}$ |
| 氣味 | 無味 |
| 密度 | 2.13 g/cm3 |
| 溶解度 | 溶於水和甘油,不溶於乙醚。 |
| 沸點 | 1388°C |
| 熔點 | 318°C |
化學性質
與酸的反應 - 當它與酸反應時,會形成鹽和水。
與金屬的反應 - 當氫氧化鈉在高溫下與金屬反應時,會形成金屬氧化物並釋放氫氣和鈉。
與酸性氧化物的反應 - 當它與酸性氧化物二氧化碳反應時,會形成碳酸鈉和水。這是一個放熱反應。
$$\mathrm{NaOH(aq)\:+\:HCl(aq)\:\rightarrow\:NaCl(aq)\:+\:H_{2}O(l)}$$
$$\mathrm{4Fe\:+\:6NaOH\rightarrow\:2Fe_{2}O_{3}\:+\:3H_{2}\:+\:6Na}$$
$$\mathrm{2NaOH\:+\:CO_{2}\rightarrow\:Na_{2}CO_{3}\:+\:H_{2}O}$$
氫氧化鈉的用途
金屬氫氧化物不溶於水,但氫氧化鈉溶於水,因此它用於水處理,沉澱金屬氫氧化物,如氫氧化鋁。
氫氧化鈉會緩慢與玻璃反應,形成矽酸鈉。
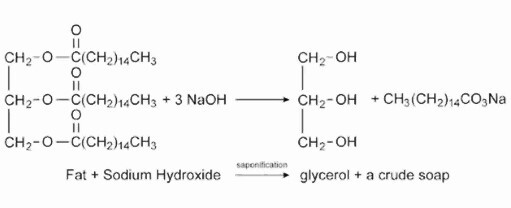
它用於皂化過程以形成洗滌劑。
$$\mathrm{6NaOH(aq)\:+\:{Al_{2}}(SO_{4})_{3}(aq)\rightarrow\:2Al(OH)_{3}(s)\:+\:3Na_{2}SO_{4}(aq)}$$
氯漂白劑是透過將氫氧化鈉與氯結合製備的。
它也用於製藥工業,用於製備抗凝劑、藥物等。
它用於燃料電池、食品防腐劑和食品加工。
與氫氧化鈉相關的健康危害
它具有高度腐蝕性,可引起嚴重的組織燒傷。
如果接觸氫氧化鈉溶液或固體,可能會引起眼睛和皮膚刺激以及皮炎。
食用或飲用氫氧化鈉可能會導致燒傷、嘔吐、噁心,甚至死亡等。
趣味知識
當我們要配製氫氧化鈉溶液時,我們總是將固體氫氧化鈉放入水中,而不是將水倒入固體氫氧化鈉中。當它溶解在水中時,會產生熱量,這些熱量被水吸收,而不是被氫氧化鈉吸收。如果我們將水倒在固體氫氧化鈉上,可能會造成燒傷。
結論
氫氧根是一種帶負電的陰離子,呈鹼性,pH值高。當它與H+離子反應時,透過形成離子鍵而中和。大多數金屬氫氧化物不溶於水,如氫氧化銅(II)或氫氧化鐵,但氫氧化鈉可溶於水。氫氧化鈉是一種無機化合物。它用於各種商業用途,例如食品工業、醫藥、實驗室等。
常見問題
1. 為什麼氫氧根離子單獨存在於水中?
氫氧根是一種帶負電的離子,即鹼,而H+離子是帶正電的酸。酸鹼會在溶液中反應並中和。因此,氫氧根離子單獨存在於水中。
2. 氫氧根離子的用途是什麼?
氫氧根離子是一種強鹼,用於許多化學反應。例如,氫氧化鉀用於農業。
3. 氫氧化鈉在造紙工業中的作用是什麼?
木材首先用氫氧化鈉和硫化鈉溶液處理。木材中不需要的物質溶解在溶液中,並純化用於製造紙張的纖維素。
4. 氫氧化鈉在土壤中的作用是什麼?
氫氧化鈉用於提高土壤的pH值。
5. 氫氧化鈉是否具有抗氧化效能?
從植物或土壤中提取的氫氧化鈉具有抗氧化效能。


 資料結構
資料結構 網路
網路 關係型資料庫管理系統 (RDBMS)
關係型資料庫管理系統 (RDBMS) 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C語言程式設計
C語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL JavaScript
JavaScript PHP
PHP