鏑
介紹
元素是一種只包含一種原子的化學物質,具有獨特的物理和化學性質。元素可以透過從地球上提取或人工合成的方式被人類發現。鏑也是一種具有其自身特性的元素。鏑於1886年由保羅·埃米爾·勒科克發現。 “鏑”這個名字來源於希臘語“dysprositos”,意為“難以獲得”。1950年,弗蘭克·斯佩丁發明了離子交換色譜法後,人們才獲得了純鏑。現在,這種稀土元素的提取是藉助液-液萃取法完成的。
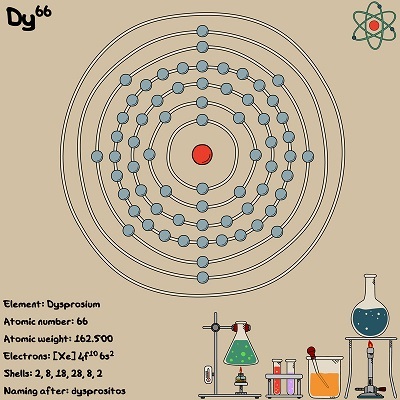
什麼是鏑?
鏑是一種f區元素,屬於鑭系元素。它位於元素週期表第六週期,原子序數為66,是一種金屬元素。它天然存在於獨居石和氟碳鈰礦等礦物中,也少量存在於磷釔礦和獨居石中。可以透過離子交換和溶劑萃取法從這些礦物中提取。
由於鏑與氧氣和水的高反應活性,其用途非常有限。與其他鑭系元素不同,鏑在自然界中並非以單質形式存在。它是一種外觀呈銀白色的軟金屬,可以用刀切割。鏑刨花燃燒時呈白熱狀態,並迅速點燃。這種元素有幾種顏色鮮豔的鹽。它與鈥一起具有最高的磁矩強度和最高的磁力方向。這種元素的丰度高於錫,全球年產量約為100噸。約99%的鏑產自中國,主要存在於中國的離子吸附粘土礦石中。
歷史
鏑於1886年由科學家保羅·埃米爾·勒科克在巴黎首次發現。但當時並沒有提取或收集這種元素。他使用了一種方法,該方法包括將氧化鏑溶解在酸中,然後在加入氨後沉澱出氫氧化物。後來,人們又用這種方法嘗試了30多次,最終將其命名為鏑。但又過了8年才成功提取這種元素。這得益於1950年離子交換色譜法的發現。在商業提取釔的過程中,它也作為副產品獲得。

W. Oelen, Dysprosium1, CC BY-SA 3.0
鏑的性質
作為一種元素,鏑的性質非常獨特,部分性質如下表所示。
| 鏑 | Dy |
|---|---|
| 原子序數 | 66 |
| 族 | 鑭系元素 |
| 區 | f區 |
| 物理狀態 | 固體 |
| 電子構型 | $\mathrm{[Xe]4f^{10}6s^{2}}$ |
| 週期 | 6 |
| 沸點 | 2567°𝐶 |
| 熔點 | 1412°C |
| 主要同位素 | $\mathrm{Dy_{164}}$ |
| 原子量 | 162.5 |
| 密度 | 8.55𝑔𝑐𝑚−3 |
| 電負性 | 1.22 |
| 共價半徑 | 1.8Å |
| 電離能 | 573.017𝑘𝐽 𝑚𝑜𝑙−1 |
| 原子半徑 | 2.31Å |
鏑的用途
鏑的用途詳述如下。
在核反應堆控制中,使用氧化鏑-鎳金屬陶瓷,因為它能輕易吸收中子且不會收縮或膨脹。
在鹵化物放電燈中使用碘化鏑。
用作合金新增劑,以提高永磁物質$\mathrm{Nd_{2}Fe_{14}B}$的居里溫度。
用於製造熒光粉啟用劑。
用於製造雷射材料。
在劑量計中,用於監測電離輻射。
在研究多種化學反應中,用作紅外輻射源。
用於製造多種合金。
用於製造具有永久磁性的材料。
用於光碟、硬碟和資料儲存應用。
鏑的化學性質
鏑金屬在乾燥空氣中非常穩定,但在潮溼空氣中會很容易轉化為氧化物。
它是一種高電正性金屬,因此即使與冷水也會 readily react readily readily 。
它也會與多種鹵素化合物反應。鏑與鹵素的反應如下所示。
鏑與硫酸反應會形成順磁性的三硫酸鏑。反應式為:
氯化鏑和氟化鏑與鈣反應併發生還原反應。反應式為:
$$\mathrm{4Dy\:+\:3O_{2}\:\rightarrow\:2Dy_{2}O_{3}}$$
因此會形成三氧化二鏑。
$$\mathrm{2Dy(s)\:+\:6H_{2}O(l)\:\rightarrow\:2Dy(OH)_{3}(aq)\:+\:3H_{2}(g)}$$
$$\mathrm{2Dy(s)\:+\:3I_{2}\:\rightarrow\:2DyI_{3}(s)}$$
而$\mathrm{DyI_{3}}$的顏色為綠色。
$$\mathrm{2Dy(s)\:+\:3H_{2}SO_{4}(aq)\:\rightarrow\:2Dy^{3+}(aq)\:+\:3SO^{2-}_{4}(aq)\:+\:3H_{2}(g)}$$
$$\mathrm{3Ca\:+\:2DyF_{3}\:\rightarrow\:2Dy\:+\:3CaF_{2}}$$
$$\mathrm{Li\:+\:DyCl_{3}\:\rightarrow\:Dy\:+\:3LiCl}$$
鏑的其他化學性質如下表所示。
| 鏑 | Dy |
|---|---|
| 比熱容 | 173 𝐽 𝑘𝑔−1 𝐾−1 |
| 電阻率 | $\mathrm{926\:n\Omega.m}$ |
| 晶體結構 | 密排六方 |
| 熱導率 | $\mathrm{10.7\frac{W}{m.K}}$ |
| 磁性排序 | 順磁性 |
氧化態和同位素
鏑常見的氧化態為+3,主要以𝐷𝑦3+存在。同位素及其原子質量如下表所示。
| 同位素 | 原子量 |
|---|---|
| $\mathrm{Dy^{164}}$ | 163.929 |
| $\mathrm{Dy^{163}}$ | 162.929 |
| $\mathrm{Dy^{162}}$ | 161.927 |
| $\mathrm{Dy^{161}}$ | 160.927 |
| $\mathrm{Dy^{160}}$ | 159.925 |
| $\mathrm{Dy^{158}}$ | 157.924 |
| $\mathrm{Dy^{157}}$ | 155.924 |
結論
鏑是一種在地球地殼中以礦物形式存在的元素。它是一種f區元素,屬於鑭系元素。它與空氣和水反應非常劇烈。它於1886年由科學家保羅·埃米爾·勒科克發現。這種元素的特性、物理和化學性質使其在磁性領域和合金製造業中得到了廣泛的應用。該元素的原子序數為66。該元素的用途非常廣泛,年產量約為100噸。其主要產地是中國。該元素常見的氧化態為+3。該元素有多種同位素。
常見問題
1. 鏑有毒嗎?
鏑的毒性取決於相應的鹽。某些可溶性鏑鹽在攝入時具有毒性。如果攝入超過500克這種化合物,就會有毒。而不可溶性鏑鹽則不是有毒化學物質。
2. 鏑在生物體中起什麼作用?
鏑在動植物中不發揮任何生物學作用。因此,它不會汙染環境。
3. 什麼是退磁?
加熱金屬以去除其磁性的過程稱為退磁。由於鏑是一種具有抗退磁特性的金屬,因此它被廣泛用作電動汽車、風力渦輪機等多種材料的合金。
4. 鏑易燃嗎?
氧化鏑和氟化鏑是非易燃化合物。
5. 鏑是導體嗎?
鏑是良好的導體,其電導率為$\mathrm{1.1\:\times\:10^6\frac{s}{m}}$。


 資料結構
資料結構 網路
網路 關係資料庫管理系統 (RDBMS)
關係資料庫管理系統 (RDBMS) 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C語言程式設計
C語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP