離子鍵、共價鍵和金屬鍵的區別
引言
鍵可以分為兩大類:主鍵和次級鍵。次級鍵與主鍵相反,是機械地將分子結合在一起。分子中的原子透過主鍵以化學方式結合在一起。三種基本型別的鍵合是金屬鍵、共價鍵和離子鍵。次級鍵的例子包括氫鍵、偶極鍵和分散鍵。主鍵比次級力更穩定,並且具有更高的鍵能。與共價鍵(透過兩個原子共享其價電子形成)不同,金屬鍵是在金屬晶格中不同型別的原子共享不同型別的電子時形成的。當一個原子將電子轉移到另一個原子時,就會形成離子鍵。這就是離子鍵、共價鍵和金屬鍵之間的主要區別。
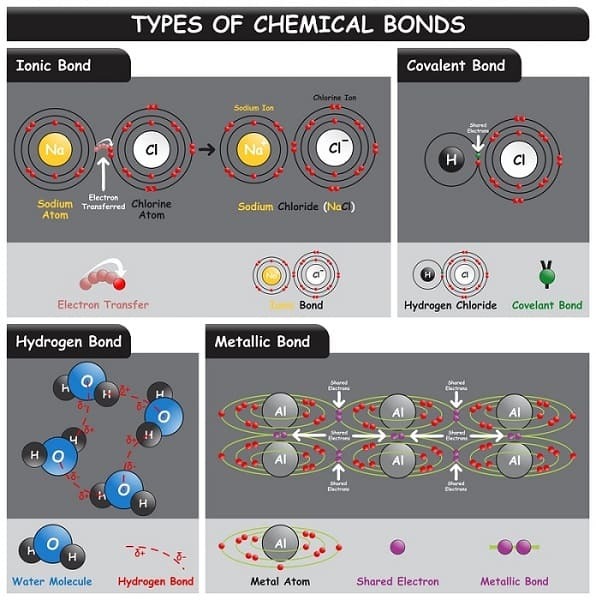
什麼是離子鍵?
某些原子經常給出或接受電子以填充其最外層軌道,這使得它們更穩定。與在外層軌道中有更多電子的原子(更喜歡接受電子併產生帶正電的離子)相反,原子最外層電子數很少的原子傾向於捐贈電子,從而導致帶正電的離子。當這些離子被放在一起時,它們的相反電荷充當吸引力。這些相互作用被稱為離子鍵。這些強鍵也稱為靜電鍵。
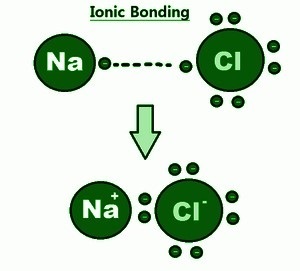
條件
具有較低電離能的金屬。
非金屬具有較高的電子親和力
鍵的晶格能更大。
金屬和非金屬之間的電負性差異更大。
較大的陽離子半徑與較小的陰離子半徑相比。
例子
𝑁𝑎𝐶𝑙、𝐵𝑒𝑂、𝐿𝑖𝐹等。
什麼是共價鍵?
當兩個原子共享價電子時,就會形成共價鍵。兩個原子的電負性彼此之間幾乎沒有差異。相同型別的原子或不同型別的原子可以彼此形成共價鍵。例如,氟需要一個電子來完成其外殼;因此,另一個氟原子透過形成共價鍵來共享此電子,從而形成F2分子。具有共價鍵的物質可以存在於所有三種狀態,即固態、液態和氣態。
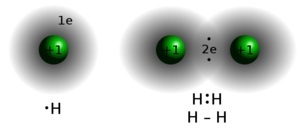
條件
兩個參與原子中的每一個都需要在其價層或最外層具有5、6或7個電子才能建立共價鍵。
結合形成共價鍵的原子之間必須存在相等的電負性差異。
結合形成共價鍵的原子應該以相等的力量相互吸引。
為了防止電子容易被去除,兩個原子的電離能都必須很高。
例子
水分子、金剛石、二氧化矽、氮氣、氫氣等。
什麼是金屬鍵?
金屬原子的原子核在金屬晶格中鬆散地容納價電子。因此,價電子與原子核分離所需的能量極低。這些電子分裂,形成帶正電的金屬原子離子。電子雲,一個由帶負電的自由移動電子的大集合,圍繞著這些帶正電的離子。離子對電子雲的吸引產生靜電力。這些相互作用被稱為金屬鍵。由於金屬晶格中的幾乎每個原子都共享一個電子,因此不可能分辨哪些原子共享哪個電子。
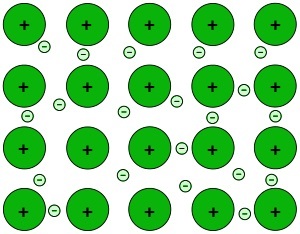
條件
單個原子通常不穩定,因此形成鍵以產生更穩定的結構。
每個原子中都存在價電子,並且可以使用元素週期表的族數來確定元素或金屬的價電子數(這對於d區元素,即過渡金屬有所不同)。
例子
幾種金屬,例如鐵、銅、金、銀和鎳。
離子鍵、共價鍵和金屬鍵的區別
| 依據 | 離子鍵 | 共價鍵 | 金屬鍵 |
|---|---|---|---|
| 形成 | 帶相反電荷的離子透過靜電相互吸引。 | 透過共享電子對 | 離域電子雲和帶正電的金屬離子透過靜電力相互吸引。 |
| 導電性 | 低導電性 | 非常低的導電性 | 高導電性 |
| 存在於…之間 | 金屬和非金屬 | 非金屬和準金屬,或兩個非金屬 | 電子雲和帶正電荷的離子 |
| 結合能 | 與金屬鍵相比,結合能更大 | 與金屬鍵相比,結合能更大。 | 與共價鍵和離子鍵相比,結合能較低。 |
| 異構現象 | 非方向性 | 方向性 | 非方向性 |
| 化合物的物理狀態 | 它僅在室溫下以固態存在。 | 在所有三種狀態下:室溫下的液體、氣體和固體。 | 僅在室溫下以固態存在 |
| 金屬特性 | 非延展性和非展性 | 非延展性和非展性 | 延展性和展性 |
| 溶解性 | 在溶液中分解成離子。 | 可以在溶液中保持其分子同一性 | 雖然某些金屬和水會發生劇烈反應,但另一些則不會 |
| 物理性質 | 較高的熔點和沸點 | 較低的熔點和沸點 | 較高的熔點和沸點 |
結論
簡而言之,當金屬和非金屬接觸時,會形成離子鍵。電子從金屬原子轉移到非金屬原子導致離子形成。兩個原子共享電子以填充其外殼,從而形成共價鍵。金屬鍵之所以特殊,是因為它發生在原子完全失去其最外層電子時。這些未結合的電子與其他金屬原子結合以形成金屬固體。最重要的結論是,共價鍵和金屬鍵導致具有不同特性的不同材料。在嘗試解決化學或物理實驗室中的問題時,瞭解這些特性可能非常有益,因為它們可以幫助您預測物質的行為方式。
常見問題解答
1. 共價鍵的三種類型是什麼?
三鍵、雙鍵和單鍵是共價鍵的三種類型。
2. 金屬鍵是共價鍵還是離子鍵?
金屬透過金屬鍵合化學地連線到其他金屬。與共價鍵或離子鍵不同,金屬鍵涉及多個正離子共享大量電子。金屬的電離能低。
3. 離子鍵和金屬鍵:哪個更強?
與離子鍵和共價鍵相比,金屬鍵稍微弱一些。當正離子和負離子結合在一起時,會形成稱為離子鍵的強靜電力。由於該鍵的非方向性,電子對任何特定原子都不產生偏向的拉力。
4. 有哪五種化學鍵?
離子鍵、共價鍵、氫鍵和金屬鍵是四種主要型別的化學鍵。兩個原子之間是否存在鍵取決於它們的電負性差異。
5. 共價鍵和金屬鍵哪個更強?
除了金剛石、矽和碳之外,共價鍵通常很弱。金屬之間具有很強的鍵合。由於晶體結構,離子鍵也相當強。


 資料結構
資料結構 網路
網路 關係資料庫管理系統
關係資料庫管理系統 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C語言程式設計
C語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP