親核試劑與親電試劑的區別
介紹
克里斯托弗·凱爾克·英戈爾德於 1933 年引入了親核試劑和親電試劑這兩個術語,取代了 A. J. 拉普沃斯引入的陰離子和陽離子這兩個詞。親電試劑一詞是由兩個詞“electro”(意為電子)和“philes”(意為喜愛)組合而成。而親核試劑一詞則來源於兩個詞“nucleus”(意為原子核)和“phile”,其中“Philos”是希臘語,意為“朋友”。這兩個術語在化學中非常重要。這些化合物參與了許多有機反應。眾所周知,親電試劑和親核試劑具有相反的行為,這是許多化學反應的驅動力。因此,這兩個術語對於更好地理解化學反應非常重要。
親核試劑概述
親核試劑是可以提供其自身上電子對的化學物質。因此,所有親核試劑都含有孤對電子。它們是富電子物質,這就是它們可以提供電子的原因。親核試劑一詞也可以分成兩個部分“Nucleo”和“philes”,意思是“親核物質”。由於它們可以提供其自身上的電子對,因此被稱為路易斯鹼。它們是含有孤對電子的中性物質或帶負電荷的物質。因此,這些化學物質在化學反應中提供電子對,並進一步導致共價鍵的形成。特定親核試劑提供電子對的程度由親核性表示,類似於鹼性。氨是親核試劑的一個例子,因為它含有孤對電子。

親核試劑的例子
由於親核試劑帶負電荷或含有孤對電子。因此,可以給出一些親核試劑的例子,例如:
所有鹵素陰離子,$\mathrm{Br^{-}\:,\:Cl^{-}\:,\:I^{-}}$
氰化物,$\mathrm{CN^{-}}$
氫氧根離子, $\mathrm{OH^{-}}$
水, $\mathrm{H_{2}O}$
氨, $\mathrm{NH_{3}}$
硫酸, $\mathrm{H_{2}SO_{4}}$
親核試劑的特徵
下面詳細討論了親核試劑必須具備的一些重要特徵。
電荷 - 親核試劑必須帶負電荷,或者即使是中性物質也必須含有孤對電子。因此,親核試劑通常是帶負電荷的物質。並且,隨著負電荷的增加,親核試劑的親核性也隨之增強。
電負性 - 由於親核試劑可以提供其自身上的電子對,因此親核試劑的電負性必須較低,才能充當更好的親核試劑。因此,親核試劑通常是電負性較低的物質。
溶劑效應 - 如果在特定化學反應中,親核試劑存在的溶劑是極性或質子溶劑,它最終會影響親核試劑的強度。因此,極性溶劑可能與親核試劑中存在的孤對電子形成氫鍵,從而降低其將自身上存在的孤對電子提供給其他物質的可能性。
空間位阻 - 親核試劑不能有空間位阻,因為它可能會影響親核反應的速率。因此,好的親核試劑的空間位阻較小。
親電試劑概述
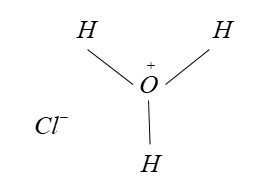
親電試劑是電子不足的化合物。因此,它們是電子缺乏的,因此可以接受電子。親電試劑一詞可以分成兩個詞,即“electro”和“philes”。合在一起,親電試劑的意思是“親電子物質”。這些化合物可能是帶正電荷的或中性的物質。這些化合物將參與親電取代反應和親電加成反應。親電試劑也稱為路易斯酸,因為它們喜歡電子對。因此,這些化學物質在化學反應中接受電子對,然後導致共價鍵的形成。親電試劑接受電子的程度由親電性表示,類似於鹼性。𝐻3𝑂+是親電試劑的一個例子。
親電試劑的例子
下面討論了一些帶正電荷或親電子物質的親電試劑的例子。
三氟化硼,$\mathrm{BF^{3}}$.
水合氫離子, $\mathrm{H^{3}O}$.
三氯化鋁, $\mathrm{AlCl^{3}}$.
鹵素分子,例如 $\mathrm{Cl^{2}\:,\:Br^{2}\:,\:F^{2}\:and\:I^{2}}$.
親電試劑的特徵
下面詳細討論了成為好的親電試劑所需的一些重要特徵。
電荷 - 親電試劑必須帶正電荷,或者它可能含有空軌道,以便在反應中從親核試劑處容納電子。
鍵型 - 親電試劑中存在的鍵必須較弱,只有這樣它才能接受電子,因此親電試劑的鍵必須是弱極性鍵。
空間位阻 - 親電試劑不能過於擁擠,只有這樣電子才能被親核試劑提供給它。
親電試劑與親核試劑的區別
親電試劑和親核試劑之間的一些區別在以下表格中列出。
| 親電試劑 | 親核試劑 |
|---|---|
| 它們通常是帶正電荷的化學物質。 | 它們通常是帶負電荷的化學物質。 |
| 它們接受電子。 | 它們提供電子。 |
| 它必須包含一個空軌道。 | 它包含一對孤對電子。 |
| 通常用 𝐸+ 表示。 | 通常用 𝑁𝑢− 表示。 |
| 缺電子物質。 | 富電子物質。 |
| 它們是路易斯酸。 | 它們是路易斯鹼。 |
| 參與親電取代和加成反應。 | 參與親核加成和取代反應。 |
| $\mathrm{BF_{3},AlCl_{2}}$ 等是例子 | $\mathrm{I^{-},Cl^{-},CN^{-}}$ 等是例子。 |
結論
化學反應是透過從一種物質到另一種物質的電子給予和接受來發生的。親電試劑和親核試劑是兩種重要的化學物質,是發生化學反應所必需的。親電試劑是帶正電荷或包含空軌道的物質,可以接受電子。而親核試劑是帶負電荷或含有孤對電子的化學物質,因此它們可以將這對電子提供給另一種物質。一些親電試劑的例子是 $\mathrm{BF_{3},AlCl_{3}}$ 等。親核試劑的例子是 𝐶𝑁−, 𝑂𝐻− 等。親電試劑和親核試劑的重要特徵受電荷、電負性、空間位阻等因素的影響。
常見問題
1. 為什麼 𝑭− 不是親核試劑?
親核試劑的親核性取決於原子的電負性。電負性是原子吸引電子對的能力。因此,電負性越強的原子,其提供的電子對就越少。由於氟是最電負性的原子,因此 F- 不是一個好的親核試劑。
2. 𝑪𝑯− 是親核試劑嗎?
𝐶𝐻− 是一個好的親核試劑,因為碳原子是一個小的原子,並且該元素保持負電荷的能力較低。因此,𝐶𝐻− 的親核性甚至高於 𝑁𝐻−
3. $\mathrm{CCl_{4}}$ 是親電試劑嗎?
$\mathrm{CCl_{4}}$ 是親電試劑,因為四氯化碳中的氯原子含有空的 d 軌道,因此可以充當親電試劑。
4. $\mathrm{PH_{3}}$ 是親核試劑還是親電試劑?
$\mathrm{PH_{3}}$,磷化氫是親核試劑,因為它含有一對孤對電子。它們可以提供其自身上的電子對。但是,當它們溶解在水中時,它們也接受水分子中存在的電子對。這個過程是水解,並導致磷酸的形成。
5. 吸電子基團對親電試劑有什麼影響?
在特定的親電試劑中存在吸電子基團會使親電試劑更具親電性。這是因為吸電子基團的連線會帶走親電試劑中已存在的電子。這將進一步使它們更具親電性。因此,吸電子基團的影響是它會增加化合物的親電性。


 資料結構
資料結構 網路
網路 RDBMS
RDBMS 作業系統
作業系統 Java
Java iOS
iOS HTML
HTML CSS
CSS Android
Android Python
Python C 語言程式設計
C 語言程式設計 C++
C++ C#
C# MongoDB
MongoDB MySQL
MySQL Javascript
Javascript PHP
PHP